Le cuivre est un métal indispensable dans de nombreuses applications industrielles, particulièrement dans le secteur de l'électricité. Sa conductivité électrique exceptionnelle en fait le matériau de choix pour les câbles, les circuits imprimés et une multitude d'autres composants électroniques. Cependant, le cuivre brut extrait des mines, souvent sous forme de "cuivre noir" ou "blister", ne possède pas la pureté requise pour ces usages de haute technologie. Ce cuivre brut contient généralement entre 98% et 99.5% de cuivre, un taux insuffisant pour répondre aux exigences de l'industrie électrique, qui demande une pureté minimale de 99.9%. C'est là qu'intervient le processus de raffinage électrolytique, une méthode sophistiquée permettant d'atteindre cette pureté élevée en séparant le cuivre des impuretés.
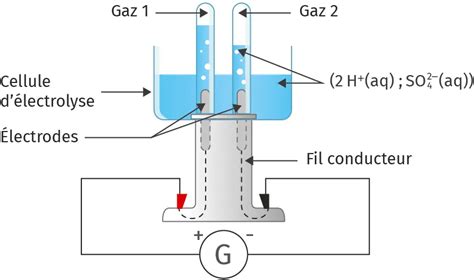
L'électrolyse est un procédé électrochimique qui utilise un courant électrique pour forcer une réaction chimique qui ne se produirait pas spontanément. Dans le cas du raffinage du cuivre, il s'agit de provoquer une réaction d'oxydoréduction. Une réaction d'oxydoréduction, également appelée réaction redox, est une réaction chimique au cours de laquelle a lieu un transfert d'électrons. Une espèce chimique dite oxydant reçoit un ou plusieurs électrons d'une autre espèce chimique dite réducteur. L'électrolyse permet donc de provoquer des transformations dites forcées en imposant une tension électrique entre deux électrodes plongées dans une solution électrolytique. Cette solution contient des ions susceptibles de participer à la réaction.
Dans le contexte du raffinage du cuivre, le cuivre brut est utilisé comme anode (l'électrode où se produit l'oxydation), tandis qu'une fine feuille de cuivre pur sert de cathode (l'électrode où se produit la réduction). Le bain d'électrolyse est une solution aqueuse de sulfate de cuivre (II) (CuSO₄) acidifiée par de l'acide sulfurique (H₂SO₄). Cette solution sert de milieu conducteur et fournit les ions cuivreux nécessaires à la réaction.
Le processus commence par la préparation des anodes. Le cuivre brut, après sa première étape de fabrication qui aboutit à la production de cuivre noir ou blister, est coulé en feuilles de 350 kg. Ces feuilles ont une surface d'environ 1 m² et une épaisseur variant entre 13 et 50 mm. Ces anodes sont ensuite placées dans un électrolyseur, qui est une cuve contenant le bain électrolytique.
Le bain d'électrolyse est soigneusement préparé pour optimiser le processus. Il est constitué d'une solution de sulfate de cuivre (II) et d'acide sulfurique. Les concentrations typiques sont d'environ 45 g.L⁻¹ pour les ions cuivre (II) (Cu²⁺) et 185 g.L⁻¹ pour l'acide sulfurique (H₂SO₄). L'acide sulfurique joue un rôle crucial en augmentant la conductivité de la solution et en empêchant la précipitation d'hydroxydes de cuivre.
L'électrolyse elle-même est réalisée dans des conditions contrôlées. La température du bain est maintenue autour de 65°C. Une tension électrique relativement basse, comprise entre 0.2 et 0.3 V, est appliquée entre l'anode et la cathode. Cette tension suffit à initier et maintenir les réactions électrochimiques souhaitées. La durée de l'électrolyse est également un facteur important, s'étendant sur une période de 21 à 28 jours. Cette longue durée permet un transfert progressif et efficace des ions cuivre de l'anode vers la cathode.
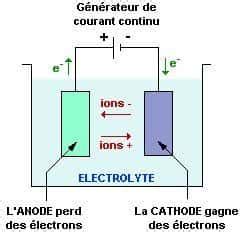
Au niveau de l'anode, le cuivre brut subit une oxydation. Les atomes de cuivre (Cu) présents dans l'anode perdent des électrons pour former des ions cuivre (II) (Cu²⁺) qui passent alors dans la solution électrolytique. La demi-équation de cette réaction est :
Cu(s) → Cu²⁺(aq) + 2e⁻
Au niveau de la cathode, qui est constituée d'une fine feuille de cuivre pur, les ions cuivre (II) présents dans la solution gagnent des électrons et se déposent sous forme de cuivre métallique pur (Cu). La demi-équation de cette réaction est :
Cu²⁺(aq) + 2e⁻ → Cu(s)
L'équation bilan globale de l'électrolyse, en considérant uniquement le cuivre, est donc la suivante :
Cu(s) (anode) → Cu(s) (cathode)
Ce processus est appelé électrolyse à anode soluble car l'anode elle-même se dissout progressivement au fur et à mesure que le cuivre pur est déposé sur la cathode.
Le raffinage électrolytique ne se limite pas au dépôt de cuivre pur. Il permet également de séparer le cuivre des impuretés présentes dans le cuivre brut. Ces impuretés peuvent être classées en deux catégories :
Impuretés moins nobles que le cuivre : Ce sont des métaux dont le potentiel d'oxydation est inférieur à celui du cuivre, comme le fer (Fe) ou le nickel (Ni). Ces métaux ont tendance à s'oxyder plus facilement que le cuivre. Ils passent donc dans la solution sous forme d'ions (Fe²⁺, Ni²⁺). Cependant, comme leur potentiel de réduction est également inférieur à celui du cuivre, ils ne se déposent pas sur la cathode. Ils restent dissous dans le bain électrolytique, contribuant à son enrichissement progressif en ces ions.
Impuretés plus nobles que le cuivre : Ce sont des métaux dont le potentiel d'oxydation est supérieur à celui du cuivre, comme l'argent (Ag), l'or (Au) ou le platine (Pt). Ces métaux ont tendance à s'oxyder plus difficilement que le cuivre. Ils ne s'oxydent donc pas à l'anode et restent sous forme solide. Au fur et à mesure que l'anode se dissout, ces impuretés solides tombent au fond de la cuve, formant une boue appelée "boues anodiques". Ces boues sont ensuite collectées et traitées séparément pour récupérer les métaux précieux qu'elles contiennent, ce qui représente une source de revenus supplémentaire significative pour les fonderies.
Le plomb (Pb) est une impureté dont le comportement dépend des conditions. Son potentiel d'oxydation est légèrement inférieur à celui du cuivre, mais il peut former des composés insolubles (sulfate de plomb) dans le bain acide, ce qui peut conduire à sa précipitation.
L'efficacité de la séparation des impuretés dépend des potentiels d'oxydoréduction des différents couples présents. Par exemple, dans l'exercice fourni, pour séparer le cuivre du plomb et de l'argent, on utilise les potentiels standards : E°(Ag⁺/ Ag(s)) = 0,80 V, E°(Cu²⁺/ Cu(s)) = 0,34 V, et E°(Pb²⁺/ Pb(s)) = -0,13 V. Le potentiel de l'anode (EA) et celui de la cathode (EC) sont ajustés pour permettre l'oxydation du cuivre tout en minimisant l'oxydation des impuretés plus nobles et la réduction des impuretés moins nobles.
Le principal avantage de cette méthode est l'obtention d'un cuivre d'une pureté exceptionnelle, atteignant 99.9% ou même 99.95%. Cette haute pureté est essentielle pour les applications électriques où même de faibles pourcentages d'impuretés peuvent altérer la conductivité et la fiabilité des composants.
Cependant, le processus de raffinage électrolytique est énergivore. La consommation d'énergie électrique est d'environ 250 kWh par tonne de cuivre raffiné. Pour illustrer l'ampleur de la production, on peut noter que pour produire 600 tonnes de cuivre par jour, on utilise 1 092 cuves d'électrolyse, chacune contenant 46 anodes.
Le calcul de l'énergie électrique consommée peut être effectué en utilisant la formule W = UIt, où U est la tension, I est l'intensité du courant et t est la durée. Pour une tonne de cuivre, avec une consommation de 250 kWh, cela représente une quantité d'énergie considérable.
Pour chaque anode soluble de cuivre brut (pesant environ 350 kg), on obtient deux cathodes de cuivre pur. Ces cathodes, initialement minces et pesant environ 8 kg, augmentent de masse jusqu'à atteindre 140 à 150 kg chacune, avec une teneur minimale de 99.9% en cuivre. Cette transformation massive illustre l'efficacité du processus de dépôt électrolytique.
Le cuivre raffiné par voie électrolytique est la pierre angulaire de l'industrie électrique et électronique moderne. Il est utilisé dans :
Au-delà de l'électrolyse pour la purification, le principe de l'électrolyse est également utilisé dans d'autres procédés industriels, tels que l'électrozingage pour la protection du fer contre la corrosion, ou pour la récupération de métaux comme l'aluminium. L'électrolyse est, en essence, l'inverse du fonctionnement d'une pile électrochimique, où une réaction spontanée produit de l'électricité.
Le raffinage électrolytique du cuivre est un exemple remarquable de l'application des principes de l'électrochimie à l'échelle industrielle. Il permet de transformer un métal d'une pureté modeste en un matériau de haute technologie, indispensable à notre société moderne. Le contrôle précis des paramètres tels que la composition du bain, la tension appliquée, la température et la durée de l'électrolyse, ainsi que la gestion astucieuse des impuretés, sont autant de facteurs qui contribuent à l'efficacité et à la rentabilité de ce processus complexe. La récupération des métaux précieux contenus dans les boues anodiques ajoute une dimension économique et environnementale supplémentaire à cette méthode de purification essentielle.
tags: #exercice #purification #du #cuivre #par #raffinage