La purification des protéines est une étape cruciale dans de nombreuses applications expérimentales, allant des études structurelles aux dosages biochimiques in vitro. L'objectif principal est d'isoler une protéine d'intérêt spécifique à partir d'un mélange complexe, tout en préservant son activité biologique et son intégrité chimique. Pour atteindre cet objectif, diverses stratégies ont été développées, parmi lesquelles la purification par étiquetage (tagging) s'est imposée comme une méthode de choix. Cette approche repose sur l'ajout d'une courte séquence d'acides aminés, ou "tag", à la protéine d'intérêt lors de sa production. Ce tag confère des propriétés spécifiques à la protéine, facilitant ainsi sa détection, sa solubilisation et, surtout, sa purification par chromatographie d'affinité.
Avec l'avènement de la biologie des systèmes, la caractérisation à l'échelle du génome des complexes macromoléculaires protéiques est devenue une pierre angulaire de la recherche. Ces complexes, définis comme des ensembles de partenaires protéiques interagissant de manière stable, jouent un rôle fondamental dans les processus cellulaires. L'identification précise et sensible des composants polypeptidiques, qu'ils soient spécifiques à un complexe ou partagés entre plusieurs, exige une purification poussée, approchant l'homogénéité. C'est dans ce contexte que les méthodes de purification par étiquetage, combinées à la spectrométrie de masse, ont pris une importance capitale.
Pour répondre à ce besoin d'isolement rapide et efficace de complexes protéiques natifs, le système de purification séquentielle par affinité (SPA) a été développé. Ce système utilise un double étiquetage d'affinité, composé de trois séquences FLAG modifiées (3X FLAG) et d'un peptide de liaison à la calmoduline (CBP), séparés par un site de clivage pour la protéase du virus de la mosaïque du tabac (TEV). L'introduction de ce SPA-tag, sous forme de cassette d'ADN flanquée de séquences ciblantes spécifiques au gène, se fait directement sur le chromosome de E. coli par recombinaison homologue. L'objectif est de produire le protéine taguée à des niveaux quasi endogènes, afin d'éviter des associations protéiques non spécifiques qui pourraient fausser les résultats. Ce protocole détaillé et optimisé permet l'identification, par spectrométrie de masse, des sous-unités de complexes protéiques bactériens, même ceux de faible abondance, dans le cadre d'études protéomiques à grande échelle.
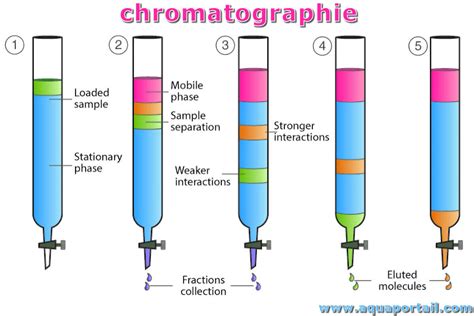
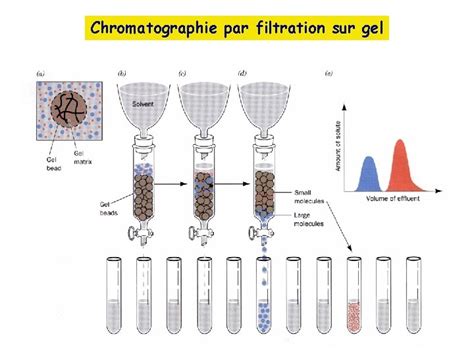
La chromatographie d'affinité est une technique puissante qui exploite les interactions moléculaires spécifiques entre une protéine d'intérêt et un ligand immobilisé sur une matrice solide. Le principe repose sur la capacité de la protéine à se lier réversiblement au ligand, permettant ainsi de la séparer d'autres composants du mélange. Les différents types de chromatographie sur colonne couramment utilisés comprennent la chromatographie d'affinité, la chromatographie d'échange d'ions (IEX), la chromatographie d'interaction hydrophobe (HIC) et la chromatographie d'exclusion stérique (SEC). Souvent, une combinaison de ces techniques est nécessaire pour atteindre la pureté requise pour les applications en aval.
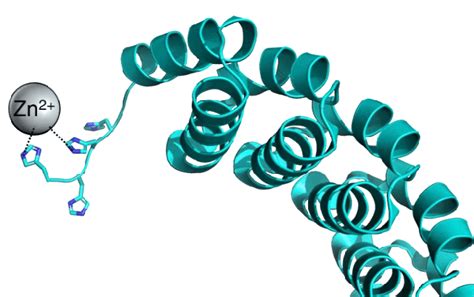
Parmi les étiquettes les plus couramment utilisées, l'étiquette polyhistidine (His-tag), une chaîne de six à neuf résidus histidine, se distingue par sa simplicité et son efficacité. Les protéines portant un His-tag se lient sélectivement à divers ions métalliques immobilisés, tels que le nickel, le cobalt ou le cuivre, dans des conditions tamponnées spécifiques. Cette affinité est exploitée dans la chromatographie d'interaction métallique affine (IMAC).
La base de cette purification réside dans la capacité des résidus histidine à chélater les ions métalliques. Les supports chromatographiques, tels que les billes d'agarose ou les particules magnétiques, sont fonctionnalisés avec des groupes chélateurs comme l'acide nitrilotriacétique (NTA) ou l'acide iminodiacétique (IDA), qui immobilisent ensuite les ions métalliques désirés. Le système le plus répandu est la résine Ni-NTA, où les ions nickel sont complexés.
L'IMAC permet des enrichissements considérables, pouvant atteindre 100 fois, en une seule étape de purification. Le nickel est le métal le plus couramment utilisé en raison de sa grande capacité de liaison. Des produits tels que le HisPur Ni-NTA Superflow Agarose de Thermo Fisher Scientific offrent une capacité de liaison dynamique élevée, idéale pour les purifications à grande échelle, permettant de récupérer plusieurs milligrammes de protéine par millilitre de résine. La purification de plus de 4 grammes de protéine 6xHis-GFP a été réalisée en seulement 3 heures en utilisant ce type de résine.
Cependant, le nickel présente une affinité pour les clusters d'histidine endogènes, ce qui peut entraîner des liaisons non spécifiques. L'ajout d'une faible concentration d'imidazole (10-25 mM) dans le tampon de liaison et de lavage aide à minimiser ces interactions parasites.
Le cobalt, quant à lui, offre une interaction plus spécifique avec les His-tags, résultant en une réduction des liaisons non spécifiques et donc une pureté accrue. La résine Thermo Scientific HisPur Cobalt Resin est un exemple de ce type de support, fournissant une haute pureté sans nécessiter d'optimisation poussée des conditions de lavage à l'imidazole.
Le cuivre, bien que se liant plus fortement aux His-tags, offre la plus grande capacité de liaison mais la plus faible spécificité, ce qui peut être problématique pour l'obtention de protéines très pures.
Les poly-His tags se lient de manière optimale aux résines IMAC dans des conditions proches de la neutralité (pH physiologique et force ionique). Un tampon typique est le Tris-buffered saline (TBS) à pH 7.2, contenant 10-25 mM d'imidazole. Il est important de noter que des agents réducteurs comme le DTT ou le TCEP, ainsi que des agents chélateurs comme l'EDTA, peuvent affecter les performances des résines Ni-IMAC classiques en arrachant le métal. Des formulations spéciales de résines Ni-IMAC, compatibles avec ces agents, sont disponibles et particulièrement utiles pour la purification de protéines sécrétées dans le milieu de culture ou nécessitant la présence d'EDTA pour leur stabilité.
L'élution des protéines capturées se fait généralement par une concentration élevée d'imidazole (au moins 200 mM), un pH bas (par exemple, 0.1 M glycine-HCl, pH 2.5), ou un excès de chélateurs puissants comme l'EDTA. L'imidazole est l'agent d'élution le plus courant.
Il faut être conscient que les immunoglobulines, en raison de la présence de multiples histidines dans leur région Fc, peuvent se lier aux supports IMAC, entraînant un bruit de fond élevé et de faux positifs si les conditions de liaison ne sont pas suffisamment strictes. De même, les albumines comme le BSA peuvent également se lier aux supports IMAC.
Une autre étiquette largement utilisée est la Glutathion S-transférase (GST). Les protéines portant un tag GST sont purifiées par chromatographie d'affinité sur des résines de glutathion immobilisé (GSH). Le principe repose sur l'interaction spécifique et covalente entre la protéine de fusion GST et le glutathion.
La résine GSTSep, par exemple, utilise un gel d'agarose couplé chimiquement au glutathion réduit via un bras de 12 atomes. Cette conception améliore l'efficacité de purification, permettant de transporter plus de 20 mg de protéine de fusion GST par millilitre de milieu. L'élution est réalisée en utilisant du glutathion libre (GSH), qui entre en compétition avec le glutathion immobilisé pour se lier à la protéine de fusion, libérant ainsi la protéine d'intérêt.
Le tag GST est particulièrement adapté à la production de protéines recombinantes dans des systèmes d'expression eucaryotes (cellules d'insectes, mammifères) ou des systèmes acellulaires, car la GST est endogène chez les eucaryotes mais absente chez les bactéries. La purification se fait par élution avec du glutathion soluble.
D'autres étiquettes d'affinité sont également disponibles et utilisées en fonction des besoins spécifiques :
Indépendamment de l'étiquette choisie, plusieurs facteurs sont essentiels pour optimiser le processus de purification :
Le choix de la méthode de purification dépendra fortement de l'application en aval de la protéine purifiée. La quantité et la pureté nécessaires doivent être suffisantes pour l'analyse expérimentale, et la conformation native et fonctionnelle de la protéine doit être prise en considération.
La purification des protéines par étiquetage, notamment grâce aux technologies SPA et IMAC, a révolutionné la manière dont les complexes protéiques sont étudiés. La combinaison de la conception d'étiquettes efficaces, de supports chromatographiques performants et d'une compréhension approfondie des principes biochimiques permet d'isoler des protéines avec une pureté et un rendement sans précédent, ouvrant la voie à des découvertes majeures en biologie moléculaire et en médecine.
tags: #purification #proteine #tag #spa