La thermodynamique, domaine fondamental de la physique, se penche sur les échanges d'énergie et les transformations de l'état de la matière. Ses applications sont vastes et touchent des secteurs aussi divers que l'industrie, la météorologie, la chimie et même la biologie. Au cœur de cette discipline se trouvent des concepts clés et des principes qui régissent le transfert et la transformation de l'énergie au sein d'un système. Comprendre ces lois est essentiel pour appréhender le monde physique qui nous entoure et optimiser l'utilisation de l'énergie dans notre vie quotidienne.
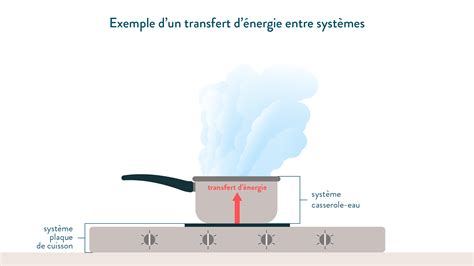
En thermodynamique, le terme "système" désigne une portion spécifique de l'univers que l'on isole pour l'étudier. Tout ce qui se trouve en dehors de ce système est appelé "l'environnement". Par exemple, lorsqu'on chauffe une casserole d'eau sur une cuisinière, le système comprend la cuisinière, la casserole et l'eau elle-même. Les transferts d'énergie se produisent à l'intérieur de ce système, entre la cuisinière, la casserole et l'eau.
Il existe deux types principaux de systèmes :
Ces définitions sont cruciales pour analyser correctement les phénomènes thermodynamiques, car elles permettent de circonscrire le champ d'étude et de quantifier les échanges d'énergie.
La thermodynamique s'articule autour de plusieurs lois fondamentales qui décrivent le comportement de l'énergie. Ces lois, bien qu'abstraites, ont des implications concrètes majeures dans de nombreux domaines.
La "quatrième loi", également connue sous le nom de loi zéro de la thermodynamique, établit le concept d'équilibre thermique. Elle stipule que si deux systèmes sont chacun en équilibre thermique avec un troisième système, alors ils sont en équilibre thermique l'un avec l'autre. Cette loi est fondamentale pour la thermométrie, car elle permet de comparer les températures de différents objets en utilisant un thermomètre comme système de référence. En d'autres termes, si un objet A a la même température qu'un objet C, et qu'un objet B a également la même température que C, alors A et B auront la même température.
Le premier principe de la thermodynamique, souvent appelé loi de la conservation de l'énergie, est l'un des piliers de la physique. Il affirme que l'énergie totale d'un système isolé reste constante au fil du temps. L'énergie ne peut être ni créée ni détruite, mais seulement transformée d'une forme à une autre.
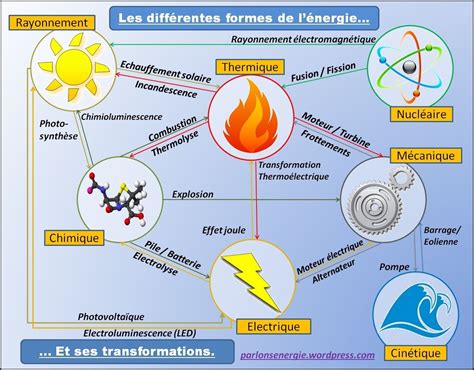
Cela signifie que pour un système donné, si de l'énergie est ajoutée ou retirée, cette modification se traduit par une variation de l'énergie interne du système. Par exemple, chauffer une bouilloire d'eau augmente son énergie interne, la portant progressivement à ébullition. Ce principe s'applique à toutes les formes d'énergie : mécanique, thermique, chimique, électrique, lumineuse, etc. Les ampoules électriques transforment l'énergie électrique en énergie lumineuse, les poêles à gaz convertissent l'énergie chimique du gaz en énergie thermique, et les plantes réalisent la transformation de l'énergie solaire en énergie chimique.
Applications Pratiques du Premier Principe :
Ce principe est essentiel dans de nombreux domaines, notamment :
L'aphorisme de Lavoisier, "Rien ne se perd, rien ne se crée, tout se transforme", résume parfaitement ce principe.
Le deuxième principe de la thermodynamique introduit le concept d'entropie, une mesure du désordre ou du caractère aléatoire d'un système. Contrairement à la première loi, celle-ci dicte que le désordre tend toujours à augmenter au cours des transformations énergétiques spontanées dans un système isolé.

L'entropie explique pourquoi certains processus naturels sont irréversibles. Par exemple, un bloc de glace fond spontanément à température ambiante, augmentant le désordre des molécules d'eau. Il faut un apport d'énergie (travail) pour transformer l'eau liquide en glace.
Conséquences du Deuxième Principe :
L'entropie est une notion clé pour comprendre la direction spontanée des processus naturels et les limites de l'efficacité énergétique.
Le troisième principe de la thermodynamique stipule qu'à mesure qu'un système approche du zéro absolu (-273,15°C), son entropie tend vers une valeur constante minimale. Ce principe permet d'établir une échelle absolue pour l'entropie et est lié à l'idée que, dans un état de température nulle, les particules d'un système seraient dans leur état d'énergie le plus bas possible, avec un désordre minimal.
Pour saisir pleinement les lois de la thermodynamique, il est essentiel de comprendre comment l'énergie circule au sein des systèmes. Les transferts d'énergie peuvent se produire de différentes manières :
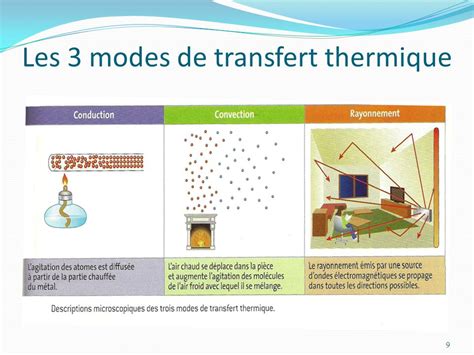
L'énergie se transforme constamment autour de nous. Ces transformations sont au cœur de nombreux processus technologiques et biologiques :
La thermodynamique utilise des fonctions d'état pour décrire l'état d'un système. Ces fonctions dépendent uniquement de l'état actuel du système, et non de la manière dont cet état a été atteint. Parmi les plus importantes, on trouve :
Ces potentiels thermodynamiques agissent comme des indicateurs de l'évolution spontanée d'un système. Un système évolue spontanément dans le sens où ces potentiels diminuent, atteignant un minimum à l'équilibre.
La thermodynamique est omniprésente dans notre vie quotidienne et dans l'industrie.
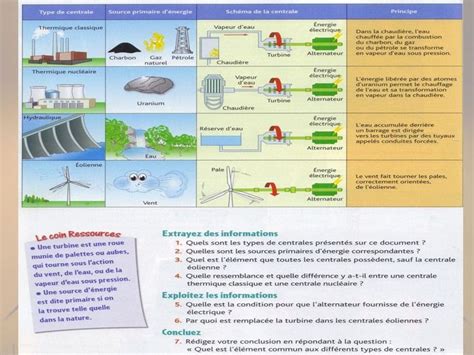
L'apprentissage de la thermodynamique, bien que parfois abstrait, est facilité par la résolution de problèmes pratiques. L'étude des gaz parfaits, par exemple, offre un cadre idéal pour des exercices. Le calcul de l'efficacité des cycles thermiques, comme le cycle de Carnot ou le cycle Otto, permet de modéliser le fonctionnement des moteurs et des turbines.
La thermodynamique classique, bien que puissante pour prédire la direction des changements spontanés, ne donne pas d'informations sur la vitesse de ces processus. C'est là qu'intervient la thermodynamique statistique, qui, en s'appuyant sur les lois de la physique microscopique, fournit des informations sur la dynamique des systèmes.
En conclusion, la thermodynamique est une science fondamentale qui régit les flux d'énergie et les transformations de la matière. Ses lois, bien que parfois complexes, sont essentielles pour comprendre le fonctionnement de l'univers, optimiser l'utilisation de l'énergie et développer des technologies plus efficaces et durables. De la simple bouilloire à la centrale électrique, en passant par les processus biologiques, les principes de la thermodynamique sont à l'œuvre, façonnant notre monde de manière profonde et continue.
tags: #la #thermodynamique #pour #les #nuls