La thermodynamique, l'étude de l'énergie et de ses transformations, est une branche fondamentale de la physique et de la chimie. Pour maîtriser ses principes, la résolution d'exercices est essentielle. Ces exercices permettent de calculer des grandeurs clés telles que l'énergie interne et l'entropie, de comparer différents types de transformations, et de comprendre les échanges d'énergie au sein de systèmes variés. Cet article explore diverses méthodes d'exercices en thermodynamique, en abordant des concepts allant de la compression d'un gaz parfait aux applications pratiques dans le corps humain et les systèmes industriels.
L'énergie interne ($U$) d'un système représente la somme de toutes les énergies microscopiques des particules qui le composent : énergie cinétique de translation, de rotation, de vibration, ainsi que l'énergie potentielle due aux interactions intermoléculaires. Pour un gaz parfait, l'énergie interne ne dépend que de sa température. Sa variation est donnée par $\Delta U = n \cdot Cv \cdot \Delta T$, où $n$ est le nombre de moles, $Cv$ la capacité thermique molaire à volume constant, et $\Delta T$ la variation de température.
L'entropie ($S$) est une mesure du désordre ou du caractère aléatoire d'un système. Elle est également liée au nombre d'états microscopiques possibles correspondant à un état macroscopique donné. La variation d'entropie lors d'une transformation réversible est définie par $\Delta S = \frac{Q{rev}}{T}$, où $Q{rev}$ est la chaleur échangée réversiblement et $T$ la température absolue. Pour une transformation irréversible, l'entropie du système et de son environnement augmente, ce qui se traduit par une entropie créée.

Les exercices en thermodynamique impliquent souvent l'étude de transformations subies par des gaz parfaits. Deux transformations fondamentales sont la compression isotherme et la compression adiabatique.
Dans une compression isotherme, la température du gaz est maintenue constante. Pour un gaz parfait, cela implique que son énergie interne reste constante ($\Delta U = 0$). Selon le premier principe de la thermodynamique ($\Delta U = Q - W$), tout le travail échangé ($W$) est compensé par un transfert de chaleur ($Q$).
Pour une compression isotherme réversible d'un gaz parfait d'un volume $V1$ à un volume $V2$ à la température $T$, le travail échangé est calculé par l'intégrale :$W{rev} = -\int{V1}^{V2} P dV$Comme $PV = nRT$ (loi des gaz parfaits), $P = \frac{nRT}{V}$.$W{rev} = -nRT \int{V1}^{V2} \frac{1}{V} dV = -nRT \ln\left(\frac{V2}{V1}\right)$
Pour une compression isotherme irréversible, le travail échangé est différent. Si la compression est effectuée rapidement contre une pression extérieure constante $P{ext}$, le travail est $W{irrev} = -P{ext}(V2 - V_1)$. En général, pour une compression irréversible, le travail est moins important (en valeur absolue) que pour une compression réversible si la pression extérieure est inférieure à la pression interne du gaz, et inversement. La comparaison du travail de compression isotherme réversible et irréversible met en évidence l'importance de la réversibilité pour minimiser le travail nécessaire (ou maximiser le travail produit lors d'une détente). La détente isotherme suit une logique similaire, où le travail produit est maximal dans le cas réversible.
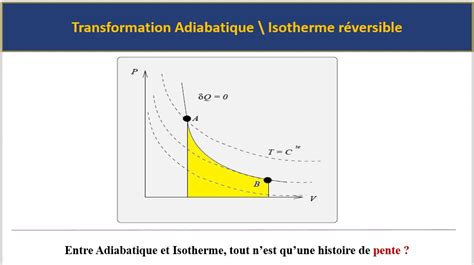
Une compression adiabatique se produit lorsque le système est isolé thermiquement de son environnement ($Q = 0$). Dans ce cas, le travail échangé est entièrement converti en variation d'énergie interne : $\Delta U = W$.
Pour un gaz parfait diatomique ($\gamma = \frac{Cp}{Cv} = \frac{7}{5}$), la relation entre la pression et le volume lors d'une transformation adiabatique réversible est $PV^\gamma = constante$.Si la compression est effectuée de manière adiabatique et réversible, du volume initial $V1$ à un volume final $V2$, la température finale $T2$ et le volume final $V2$ peuvent être calculés à partir des relations :$\frac{T2}{T1} = \left(\frac{V1}{V2}\right)^{\gamma-1}$ et $T2 V2^{\gamma-1} = T1 V1^{\gamma-1}$.
Le travail échangé lors d'une compression adiabatique réversible est :$W{rev} = \Delta U = n Cv (T2 - T1)$.Ce travail peut être exprimé en fonction des températures finale et initiale : $W{rev} = \frac{P2 V2 - P1 V_1}{1-\gamma}$.
La comparaison avec la compression isotherme montre que pour un même rapport de compression, la température augmente lors d'une compression adiabatique, car le travail fourni est entièrement converti en énergie interne. Inversement, lors d'une détente adiabatique, la température chute.
Des exercices plus élaborés peuvent impliquer des mélanges de gaz ou des systèmes divisés en plusieurs compartiments.
Considérons un cylindre divisé en deux compartiments $A$ et $B$ par un piston. Initialement, les deux compartiments contiennent chacun une mole de gaz parfait à la même pression $P0$ et température $T0$. Si le piston est mobile sans frottement et que les parois sont athermanes, le système peut subir diverses transformations.
Par exemple, si le compartiment $A$ est chauffé de manière isotherme et réversible, tandis que le compartiment $B$ subit une détente adiabatique réversible, on peut calculer les variations d'énergie interne, les travaux échangés par chaque gaz et par le système dans son ensemble.
La variation d'énergie interne du gaz dans $A$ peut être nulle si la transformation est isotherme. Dans le cas d'une détente adiabatique dans $B$, l'énergie interne diminue. Le travail total échangé par le système dépendra de la somme des travaux réalisés dans chaque compartiment.
Une détente d'un gaz dans le vide (détente de Joule) est un cas particulier de transformation irréversible. Si le gaz est parfait et que la détente est effectuée dans une enceinte calorifugée, l'énergie interne du gaz ne change pas, car il n'y a pas de travail échangé ($\Delta U = 0$ et $W = 0$). Par conséquent, la température du gaz reste constante.
Cependant, l'entropie du gaz augmente car le désordre du système croît lorsque le gaz occupe un volume plus important. Le calcul de l'entropie créée lors de cette évolution est un point clé de ce type d'exercice.
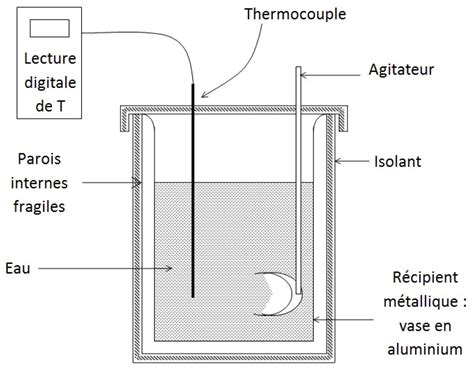
La calorimétrie est la science de la mesure des échanges thermiques. Les exercices dans ce domaine visent à déterminer des capacités thermiques, des chaleurs latentes ou à analyser des mélanges.
Un exercice typique consiste à mélanger des corps à différentes températures dans un calorimètre pour atteindre une température d'équilibre. En appliquant le principe de conservation de l'énergie (bilan énergétique), on peut établir des équations pour calculer les inconnues. Par exemple, en mélangeant de l'eau à différentes températures, on peut déterminer la capacité thermique massique de l'eau.
La détermination de la chaleur latente de vaporisation ($L{vap}$) peut se faire en chauffant une masse d'eau et en mesurant l'énergie fournie. La relation $E = L{vap} \cdot m$ permet alors de calculer $L_{vap}$.
Les exercices peuvent aussi porter sur les transferts de chaleur à travers des matériaux isolants, comme la laine de verre ou le double vitrage. La conductivité thermique ($\lambda$) et la résistance thermique sont des paramètres importants. Pour une paroi plane d'épaisseur $e$ et de surface $S$, le flux de chaleur est donné par $\Phi = \frac{\lambda S \Delta T}{e}$.
Dans le cas d'un double vitrage, la résistance thermique totale est la somme des résistances thermiques de chaque couche de verre et de la couche d'air intercalaire. La comparaison de la résistance thermique d'un double vitrage avec celle d'un mur en béton permet d'évaluer leur efficacité isolante.
La thermodynamique trouve des applications dans de nombreux domaines, y compris le corps humain, les appareils ménagers et les centrales énergétiques.
Le corps humain peut être étudié d'un point de vue thermodynamique. Il reçoit de l'énergie sous forme d'alimentation ($E{alim}$) et produit du travail mécanique ($W{méca}$) et de la chaleur ($Q$). La relation $W{méca} + Q$ permet au corps de réaliser son métabolisme. Le signe de $E{alim}$ est positif, car il s'agit d'une énergie reçue. La capacité thermique d'un être humain moyen ($C \approx 214 \text{ kJ} \cdot \text{K}^{-1}$) permet d'estimer la variation de température lors d'échanges thermiques. L'inspiration d'air par cycle respiratoire (environ 0,5 L) est également un exemple de transfert de matière et d'énergie.
Dans les centrales électronucléaires, l'énergie thermique libérée par la fission de l'uranium est convertie en énergie électrique. Le circuit de refroidissement est crucial pour évacuer l'énergie non convertie et maintenir la sécurité. Le travail électrique fourni ($W$) est lié à l'énergie thermique reçue du cœur ($Q$) et à l'énergie évacuée par le circuit de refroidissement ($Q'$).
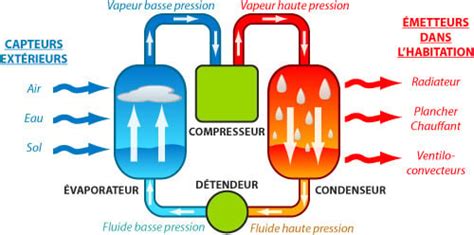
Les pompes à chaleur (PAC) sont des systèmes qui utilisent un travail ($W$) pour transférer de la chaleur d'une source froide vers une source chaude. Leur efficacité est mesurée par le coefficient de performance (COP).
Certains exercices explorent la relation entre l'énergie mécanique et l'énergie thermique, notamment lors de freinages ou de mouvements de pistons.
Lors du freinage d'une voiture, l'énergie cinétique est dissipée sous forme de chaleur au niveau des freins. Si l'on considère le système {voiture + environnement} isolé, la variation d'énergie cinétique est égale à la chaleur dégagée : $\Delta Ec = -W{freinage}$. La masse des disques de frein et leur capacité thermique massique sont utilisées pour calculer l'augmentation de température des freins.
Des exercices impliquent un cylindre fermé contenant un gaz et divisé par un piston mobile. L'ajout ou le retrait de masses sur le piston, ainsi que des transformations du gaz (isotherme, isobare, isochore, adiabatique), permettent d'étudier les échanges de travail et de chaleur, ainsi que les variations d'état du gaz. L'expression et le calcul du travail échangé par le système avec l'extérieur sont des objectifs fréquents.
La résolution d'exercices en thermodynamique est une démarche progressive qui permet d'assimiler des concepts théoriques complexes. De la compréhension des définitions fondamentales de l'énergie interne et de l'entropie, à l'analyse des transformations des gaz parfaits, en passant par les applications pratiques de la calorimétrie et des systèmes énergétiques, chaque exercice contribue à une meilleure appréhension de cette science. L'utilisation de formules appropriées, la prise en compte de la réversibilité des transformations et l'application rigoureuse des principes de conservation de l'énergie et de la matière sont les clés d'une résolution réussie.
tags: #methode #exercice #thermodynamique