En thermodynamique industrielle, divers processus régissent le comportement des gaz, et le processus isobare en est une composante cruciale. Une compréhension fondamentale de la thermodynamique exige l'exploration de processus critiques tels que le processus isobare. Les propriétés des gaz soumis à un processus isobare révèlent des modèles de comportement intrigants. Le terme "isobare" est dérivé des mots grecs "iso" signifiant "égal" et "baros" signifiant "poids". Dans un processus isobare, la pression reste inchangée, quelles que soient les variations de volume ou de température.
Le processus isobare se distingue principalement des autres processus de transfert thermique par sa condition de pression constante. Sur le plan technique, la caractérisation du processus isobare est mieux appréhendée en examinant la première loi de la thermodynamique, qui stipule que l'énergie ne peut être ni créée ni détruite. En gardant cette loi à l'esprit, la quantité totale d'énergie à l'intérieur d'un système doit rester constante, à moins que de l'énergie ne soit ajoutée ou retirée. Ainsi, toute énergie entrant dans un système doit soit augmenter l'énergie interne du système, soit effectuer un travail sur l'environnement du système.
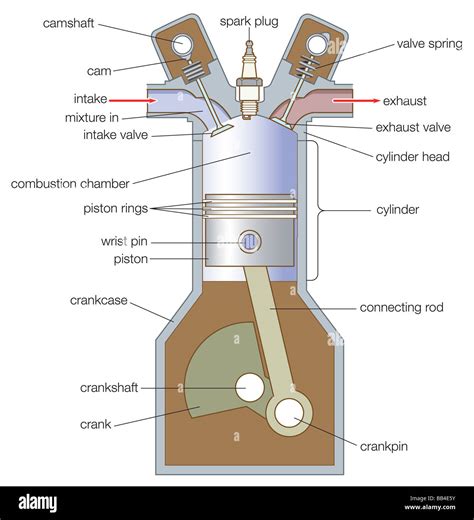
Cette situation s'apparente au chauffage d'un gaz à l'intérieur d'un piston. Si l'on applique de la chaleur sous une pression constante et que l'on laisse le gaz se dilater, le piston effectue un travail en soulevant une charge placée sur lui. De tels processus sont omniprésents dans des domaines de l'ingénierie tels que l'ingénierie mécanique, chimique et environnementale. Par conséquent, la compréhension de ces principes est essentielle à votre progression et à votre application dans votre domaine d'études.
Enfin, il convient de souligner que le processus isobare est l'un des nombreux processus élémentaires que vous rencontrerez dans le vaste domaine de la thermodynamique de l'ingénierie. Le processus isobare possède de nombreuses applications dans le monde réel, que vous rencontrez consciemment ou inconsciemment. L'essentiel de ces applications réside dans la possibilité de contrôler des températures et des volumes variables sous une pression constante pour faciliter la production de travail dans un système.
Sans le savoir, vous rencontrez plusieurs exemples de procédés isobariques chaque jour. Analogue à la mécanique d'un autocuiseur, une chaudière à vapeur utilise également les principes d'un processus isobare. À l'intérieur d'une chaudière à vapeur, l'eau est chauffée à une pression constante pour la transformer en vapeur. Ce principe repose sur la logique selon laquelle, sous une pression constante, l'augmentation de la température entraînera l'expansion du volume de l'eau, qui se transformera ainsi en vapeur, un processus au cœur de la plupart des cuisines du monde.
Considérez une pompe à vélo comme un autre exemple typique. Lorsque vous pompez de l'air dans un pneu de vélo, le volume d'air sous le piston de la pompe à vélo augmente tandis que la pression reste constante. Les processus isobariques ne jouent pas seulement un rôle d'infrastructure dans votre vie quotidienne, mais servent également de colonne vertébrale à notre économie moderne en général.
Les centrales électriques et les moteurs à combustion, par exemple, utilisent le processus isobare pour produire de l'électricité et alimenter les véhicules. Dans les centrales électriques, la vapeur produite par chauffage isobare est utilisée pour faire tourner des turbines et produire de l'électricité. Au cœur de nombreux systèmes d'ingénierie se trouvent des processus isobariques. Dans les enceintes industrielles, où le confinement de substances sous pression, généralement des gaz ou des vapeurs, joue un rôle important, le processus isobare est fondamental. Les turbines industrielles sont conçues pour extraire l'énergie d'un fluide en mouvement afin de générer un courant électrique.
À partir de ces exemples, il devient évident que le processus isobare est un aspect fondamental non seulement dans vos cours d'ingénierie, mais aussi dans le monde qui vous entoure. Les procédés isobariques figurent en bonne place dans toute une série d'applications pratiques, principalement dans le domaine industriel. La capacité à contrôler les changements de volume et de température à pression constante est à la base de nombreux systèmes naturels et artificiels.
Dans les applications industrielles, le processus isobare occupe le devant de la scène, facilitant des fonctions essentielles. Principe clé des transferts d'énergie thermique, les propriétés des processus isobares influencent le fonctionnement, la conception et les performances des systèmes technologiques. Prenons l'exemple des turbines à vapeur, pierre angulaire de la production d'énergie et des applications d'entraînement mécanique. Le fonctionnement de ces types de turbines repose fondamentalement sur des processus isobares qui convertissent l'énergie thermique en énergie mécanique. La vapeur utilisée pour entraîner les pales de la turbine est produite par des chaudières grâce à un processus isobare, dans lequel l'eau subit un changement de phase pour devenir de la vapeur à pression constante.
Dans le domaine de la thermodynamique, le processus isobare fournit un cadre théorique permettant de comprendre comment se produisent les transferts et les conversions d'énergie. La première loi de la thermodynamique, qui postule la conservation de l'énergie dans un système fermé, devient une balise pour l'application des processus isobariques dans l'analyse énergétique. Dans le cadre du processus isobare, le volume d'un système peut augmenter ou diminuer sans que la pression ne soit affectée. Par conséquent, le travail effectué est divisé en deux : le transfert de chaleur dans le système et le changement d'énergie interne du système.
La formule fondamentale de la première loi de la thermodynamique est :
[ \Delta U = Q - W ]
Où :
Selon les conditions spécifiques ou l'état de la matière du système, les applications potentielles des processus isobares peuvent varier. Par exemple, tout système impliquant un changement de phase (solide à liquide, liquide à gaz ou inversement) à pression constante, comme la fonte de la glace ou l'ébullition de l'eau, utilise intrinsèquement le processus isobare.
Les processus isobariques continuent d'orienter les progrès dans les technologies émergentes. En exploitant les changements de température et de volume sous une pression constante, les ingénieurs annoncent des améliorations sans précédent dans des domaines tels que les énergies renouvelables, la science des matériaux et le génie chimique. Par exemple, dans la production d'énergie renouvelable avec les systèmes d'énergie solaire concentrée (CSP), les fluides de transfert de chaleur comme le sel fondu sont exploités pour leurs propriétés dans des conditions isobares, ce qui permet un stockage et une utilisation efficaces de l'énergie.
En génie chimique, les processus isobares s'avèrent cruciaux dans les réactions biochimiques qui se produisent dans des cuves pressurisées comme les autoclaves. Dans ce cas, les réactions hautement exothermiques produisent de la chaleur, entraînant une augmentation de la température et une éventuelle augmentation du volume (en fonction de la réaction), mais la pression reste constante en raison de la cuve pressurisée. Les technologies émergentes, comme la production de nanomatériaux, bénéficient également des propriétés des processus isobariques. Les nanomatériaux sont souvent synthétisés dans des conditions isobariques car ils nécessitent une température et une pression spécifiques pour maintenir l'intégrité structurelle pendant la fabrication.
Sans aucun doute, l'influence des processus isobariques met en évidence l'importance des principes thermodynamiques, non seulement sur le plan théorique, mais de façon plus cruciale, dans les applications pratiques, en fournissant des solutions pour les défis d'aujourd'hui et en formant la base des progrès technologiques futurs.
Pour comprendre les mécanismes qui sous-tendent la thermodynamique, il faut s'attaquer à la formule du processus isobare. Cette formule est essentielle pour comprendre comment les changements de température et de volume d'une substance, maintenue à une pression constante, peuvent influencer sa dynamique énergétique. Si l'on se penche sur la dérivation de la formule du processus isobare, il est fondamental de comprendre que la relation est tirée des concepts de la première loi de la thermodynamique, qui stipule que l'énergie ne peut être ni créée ni détruite ; elle peut seulement être transférée ou convertie.
En appliquant cette philosophie à la première loi de la thermodynamique, le changement d'énergie interne ( (\Delta U) ) d'un système est donné par la différence entre la chaleur transférée dans le système ( (Q) ) et le travail effectué par le système ( (W) ).
La formule du processus isobare incarne implicitement plusieurs concepts mathématiques, dont le principal est le concept de changement, désigné par ( \Delta ). Cela signifie que la pression et les autres paramètres ne sont pas stationnaires ; ils évoluent au cours du processus et leur changement peut être analysé mathématiquement. Les conventions de signes utilisées dans l'équation ont également une signification importante.
Pour consolider votre compréhension de la formule, voyons comment l'utiliser à l'aide d'un exemple simple : Imaginez une chaudière à vapeur où l'eau est chauffée pour devenir de la vapeur à pression constante (un processus isobare). Disons que la chaleur fournie au système est de 1000 J et que le travail effectué par le système (sous la forme de vapeur poussant contre le couvercle du récipient) est de 400 J. Nous appliquerions alors ces chiffres dans la formule pour révéler le changement d'énergie interne : ( \Delta U = 1000 \text{ J} - 400 \text{ J} = 600 \text{ J} ).
Un processus isobare est un processus thermodynamique qui fonctionne à pression constante, c'est-à-dire que la pression reste inchangée tout au long du processus. La quintessence d'un processus isobare est l'ébullition de l'eau dans un récipient ouvert à une certaine altitude, où l'eau passe de l'état liquide à l'état gazeux tout en maintenant une pression atmosphérique constante.
La transition entre les états d'énergie dans un processus isobare dépend en grande partie du mécanisme de transfert de chaleur en vigueur. Chaque mécanisme englobe des lois fondamentales de la thermodynamique, établissant la structure du processus isobare. Trois formes principales de transfert de chaleur entrent en jeu lors de l'analyse d'un processus isobare : la conduction, la convection et le rayonnement.
Même si chaque mécanisme a sa propre fonction de transfert de chaleur, les trois fonctionnent généralement simultanément au cours d'un processus isobare. La chaleur fait partie intégrante des processus isobariques, car elle est à l'origine du changement d'état ou de la transformation du volume observés dans ces phénomènes.
La formule décrivant la chaleur transférée dans un processus isobare pour un gaz parfait est :
[ Q = n C_p \Delta T ]
Où :
Cette formule souligne que, dans un processus isobare, la chaleur transférée est directement proportionnelle à la masse de la substance, à l'ampleur du changement de température et à la nature de la substance telle qu'elle est représentée par sa capacité thermique spécifique.
On peut trouver plusieurs exemples soulignant l'impact potentiel du transfert de chaleur dans un processus isobare. Prenons le cas d'un moteur de voiture. Au cours de la course de puissance du cycle d'un moteur, l'explosion du mélange carburant-air se produit dans le cylindre, forçant le piston à descendre tout en maintenant une pression presque constante. C'est un exemple de processus d'expansion isobare, où le transfert de chaleur de la combustion du mélange air-carburant vers le piston et les parois du cylindre joue un rôle central.
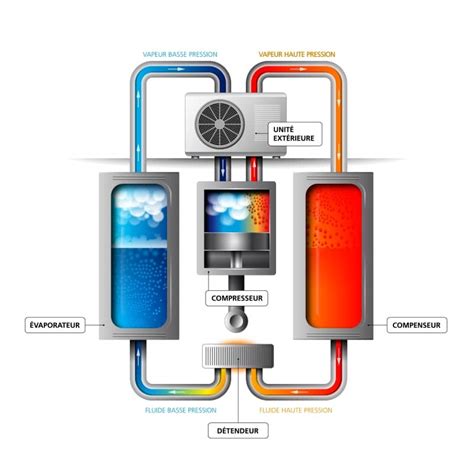
Un autre exemple peut être observé dans les systèmes de climatisation. Dans la section de l'évaporateur, le réfrigérant subit un processus isobare au cours duquel il s'évapore d'un état liquide à un état gazeux à pression constante, absorbant la chaleur de l'air ambiant au cours du processus, ce qui a pour effet de le refroidir. Ces exemples élucident la relation entre le transfert de chaleur et le processus isobare, ainsi que son énorme impact sur notre vie quotidienne et sur la technologie.
Les systèmes de chauffage et de climatisation réversibles, tels que les pompes à chaleur, exploitent les principes des processus thermodynamiques pour réguler la température intérieure. Tous les types de pompe à chaleur peuvent être utilisés en mode réversible. Cependant, si l'on considère les modèles air/air, leur principe de fonctionnement est semblable à celui d'un climatiseur puisqu'elles puisent et renvoient leur chaleur dans l'air. On les classifie donc comme des climatiseurs réversibles.
Les autres PAC (géothermiques et aérothermiques) existent également en mode réversible : elles produisent du chauffage et rafraîchissent votre intérieur. Elles fonctionnent sur un principe unique en mode chauffage : récupération des calories présentes dans le milieu extérieur naturel (sol, nappe phréatique, air) et restitution de cette chaleur à l'intérieur de l'habitation.
En mode climatisation, ce cycle est inversé : récupération de la chaleur contenue dans l'air du domicile et expulsion de ces calories vers l'extérieur.
Pour pouvoir comparer les performances des appareils, deux indicateurs sont disponibles : le coefficient de performance saisonnier (SCOP) pour la génération de chaleur et l'efficacité frigorifique saisonnière (SEER) pour la production de froid.
Le SCOP (en anglais, Seasonal Coefficient Of Performance) se calcule en divisant l'énergie calorifique produite pendant une saison (en kWh) par la quantité d'énergie consommée pendant cette même période (en kWh). La valeur du SCOP est fournie sur l'étiquette énergétique des équipements en utilisant des lettres allant de A+++ (excellente performance) à G. Le calcul du SCOP diffère selon la situation géographique avec trois climats européens choisis comme référence : Helsinki (froid), Strasbourg (tempéré) et Athènes (chaud).
L'efficacité frigorifique saisonnière est mesurée avec l'indicateur SEER (en anglais, Seasonal Efficiency Energy Ratio).
La centrale de traitement d'air Biddle améliore la qualité de l'air tout en réduisant la consommation d'énergie, grâce à la technologie de contrecourant. La chaleur résiduelle est extraite de l'air chaud pollué sortant du bâtiment et est transmise à l'air frais neuf entrant. En association avec le régulateur du système de gestion technique centralisée (GTC) du bâtiment sur le site, la centrale de traitement d'air ajuste automatiquement la vitesse du ventilateur afin de maintenir une qualité d'air optimale en fonction des données fournies par les capteurs de CO2 situés à l'intérieur du bâtiment. Quatre modèles sont disponibles : le air2air HR12 (1200m³/h), le air2air HR25 (2500m³/h), le air2air HR35 (3500m³/h) et le air2air HR45 (4500m³/h).
D'autres solutions comme les aérothermes et refroidisseurs d'air économes en énergie de la gamme NOZ, qui assurent le confort dans les pièces ayant une grande hauteur sous plafond, ou les cassettes Comfort Circle, qui associent chauffage, rafraîchissement et ventilation dans un unique bloc encastrable, font partie de l'offre. La gamme de séparateurs climatiques et de ventilo-convecteurs Biddle respecte parfaitement la toute dernière législation européenne et est en mesure de réduire de plus de 90 % les émissions de CO2 liées au chauffage et à la ventilation.
Dans le contexte de la thermodynamique, la distinction entre transformations réversibles et irréversibles est fondamentale. Les transformations réversibles d'un système sont des transformations idéales qui jouent un rôle important dans les processus thermodynamiques. Elles sont caractérisées par le fait qu'elles peuvent être inversées sans laisser de changement net dans le système ou son environnement.
Dans les systèmes fermés, la masse de matière enfermée peut subir différentes transformations. La plupart des processus thermodynamiques sont réalisés dans des systèmes ouverts où un fluide (de débit massique (qm)) entre dans le système et le quitte, souvent en négligeant l'énergie potentielle ((Ep = 0)) dans le système. Dans les systèmes ouverts, on distingue entre les processus d'écoulement et de travail.
Une transformation isobare n'est pas nécessairement réversible. La notion de réversibilité est liée à la quasi-staticité du processus, c'est-à-dire qu'il se déroule de manière suffisamment lente pour que le système soit toujours en équilibre thermodynamique, ainsi qu'à l'absence de phénomènes dissipatifs comme le frottement ou les transferts de chaleur irréversibles. Une transformation isobare peut être réversible si elle est effectuée lentement et sans frottement, par exemple, en chauffant un gaz dans un cylindre avec un piston mobile de masse négligeable, où la chaleur est ajoutée de manière progressive et l'expansion est quasi statique.
Un exemple concret de transformation réversible serait le chauffage d'un gaz dans un cylindre fermé par un piston mobile sans frottement. Si la chaleur est ajoutée de manière très lente, le gaz se dilate à pression constante, effectuant un travail sur le piston. Le processus est réversible car il peut être inversé en retirant lentement la chaleur, ramenant le piston à sa position initiale sans altération nette du système ou de son environnement.
En résumé, le chauffage isobare réversible à récupération de chaleur combine les principes fondamentaux du processus isobare avec la notion de réversibilité pour optimiser l'efficacité énergétique, particulièrement dans les systèmes de chauffage et de climatisation modernes.
tags: #chauffage #isobare #reversible #dans #un #recuperateur