La muramidase, une enzyme capable de dégrader la paroi cellulaire bactérienne, joue un rôle crucial dans divers processus biologiques, allant de la défense immunitaire à la pathogenèse bactérienne. L'analyse de la purification de la muramidase et de ses propriétés est essentielle pour comprendre son fonctionnement et son potentiel d'application. Cette exploration se penchera sur les avancées dans la purification de la lysozyme issue du lait de bufflonne, ses caractéristiques biochimiques et son spectre antibactérien, ainsi que sur le rôle spécifique d'une muramidase, TtsA, dans la sécrétion de la toxine typhoïde par Salmonella Typhi.
La lysozyme, une enzyme de type muramidase, est présente dans diverses sources biologiques, notamment le lait. Des recherches approfondies ont été menées sur la purification de la lysozyme issue du lait de bufflonne pour en élucider les propriétés. La procédure de purification a utilisé une combinaison de chromatographie d'échange d'ions sur CM-cellulose et de chromatographie d'exclusion stérique sur Sephadex G-50. Cette méthode a permis d'atteindre une purification de 8622 fois et une récupération de 39,3 % de la lysozyme.
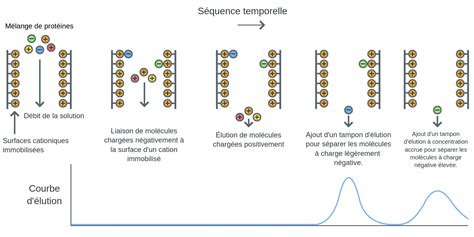
L'analyse par électrophorèse sur gel de polyacrylamide avec dodecyl sulfate de sodium (SDS-PAGE) et par électrophorèse native a confirmé la pureté homogène de l'enzyme purifiée, qui migrait sous forme d'une seule bande. La pureté immunologique de la préparation de lysozyme a été vérifiée par immunoélectrophorèse, garantissant l'absence d'autres protéines contaminantes.
Le poids moléculaire de la lysozyme du lait de bufflonne, déterminé par SDS-PAGE, s'est avéré être de 16 kDa. La composition en acides aminés de cette enzyme a été élucidée par chromatographie liquide haute performance en phase inverse (HPLC). L'analyse de la séquence des 23 premiers acides aminés N-terminaux a révélé une homologie de 56,5 % avec la lysozyme du lait de vache et de 30,4 % avec celle du lait de jument.
Une découverte significative concerne l'activité spécifique de la lysozyme du lait de bufflonne, qui s'est avérée être dix fois supérieure à celle de la lysozyme du lait de vache. De plus, la lysozyme de bufflonne a démontré une activité sur une large gamme de pH, bien que son activité ait été fortement influencée par la molarité du milieu. Ces propriétés suggèrent un potentiel d'application clinique et industrielle accru pour la lysozyme de bufflonne.
Au-delà de ses rôles bénéfiques, les muramidases sont également impliquées dans des processus pathogènes. La toxine typhoïde est un facteur de virulence majeur pour l'agent pathogène bactérien Salmonella Typhi, responsable de la fièvre typhoïde chez l'homme. Après sa synthèse par des bactéries intracellulaires, la toxine typhoïde est sécrétée dans la lumière du vacuole contenant Salmonella par un mécanisme de sécrétion strictement dépendant de TtsA.
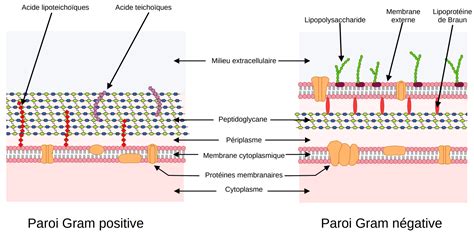
TtsA est une muramidase spécialisée dont la fonction est de faciliter le transport de la toxine à travers la couche de peptidoglycane de la paroi bactérienne. Cette couche, composée de chaînes de glycan de N-acétylglucosamine (GlcNAc) et d'acide N-acétylmurique (MurNAc) liées par des liaisons β-(1,4) glycosidiques, forme une structure rigide essentielle à la survie bactérienne. Les chaînes de glycan sont interconnectées par de courts peptides, qui sont réticulés par des transpeptidases spécifiques. La plupart de ces réticulations sont des liaisons D-D entre le groupe carboxyle du D-Ala en position 4 et le groupe ε-amino du résidu m-Dap en position 3. Cependant, des réticulations L-D, bien que moins abondantes, peuvent également se produire entre deux résidus m-Dap de peptides adjacents.
Des études antérieures ont démontré que TtsA exerce sa fonction aux pôles bactériens et nécessite l'activité de YcbB, une transpeptidase bactérienne responsable de l'introduction des réticulations L-D dans les peptides qui lient les chaînes de glycan du peptidoglycane. Les réticulations L-D étant probablement limitées à des sous-domaines spécifiques de la couche de peptidoglycane, la spécificité du substrat de TtsA semble restreindre topologiquement son activité. Cette hypothèse est soutenue par le fait que le remodelage du peptidoglycane médié par TtsA et la sécrétion de la toxine typhoïde se produisent exclusivement aux pôles bactériens.
Bien que la localisation polaire et la dépendance à YcbB de TtsA soient établies, les mécanismes précis par lesquels TtsA reconnaît son substrat et se localise aux pôles bactériens restaient inconnus. Une étude récente a identifié le domaine spécifique de TtsA qui cible son activité vers le peptidoglycane réticulé L-D aux pôles bactériens.
Pour élucider ces mécanismes, des protéines chimériques ont été construites en combinant des parties de TtsA et de Sen1395, une homologue proche de TtsA de Salmonella Enteritidis qui présente une spécificité de substrat différente et est incapable de compléter un mutant S. Typhi ∆ttsA pour la sécrétion de la toxine typhoïde. L'analyse de ces chimères a révélé que la moitié carboxy-terminale de TtsA (acides aminés 93-180) est essentielle pour la reconnaissance du substrat et la localisation polaire. Une chimère composée de la moitié amino-terminale de Sen1395 (contenant le domaine catalytique) et de la moitié carboxy-terminale de TtsA a rétabli la translocation de la toxine typhoïde à travers la couche de peptidoglycane, indiquant que ce domaine carboxy-terminal confère la spécificité du substrat et la fonction de sécrétion.
De plus, la structure atomique de TtsA liée à son substrat et celle d'une homologue proche avec une spécificité différente ont été résolues. La comparaison de ces structures a permis d'identifier les déterminants structurels spécifiques impliqués dans la reconnaissance du substrat. Ces déterminants sont situés dans le domaine carboxy-terminal de TtsA et sont responsables de sa spécificité pour le peptidoglycane réticulé L-D.
La spécificité de substrat de TtsA pour le peptidoglycane réticulé L-D a des implications importantes pour sa fonction. Le peptidoglycane réticulé L-D est principalement trouvé aux pôles bactériens, ce qui explique la localisation polaire de TtsA. L'expression d'une chimère TtsA-Sen1395, contenant le domaine carboxy-terminal de TtsA, a démontré une localisation polaire et une capacité à remodeler le peptidoglycane aux pôles, corrélant avec sa capacité à compléter un mutant S. Typhi ∆ttsA.
Il a été observé que la proportion de réticulations L-D augmente considérablement lorsque les bactéries sont cultivées dans un milieu mimant les conditions intracellulaires de Salmonella. Par conséquent, TtsA purifié n'est pas capable d'hydrolyser le peptidoglycane isolé de bactéries cultivées dans des conditions standard, mais il hydrolyse efficacement le peptidoglycane obtenu après croissance dans ce milieu spécifique.
En revanche, Sen1395 purifié a pu hydrolyser le peptidoglycane isolé de souches sauvages et mutantes, qu'elles soient cultivées dans des conditions standard ou dans le milieu spécifique, bien que dans une moindre mesure pour ce dernier. Cependant, Sen1395 purifié n'a pas réussi à hydrolyser le peptidoglycane isolé d'une souche surexprimant YcbB, et contenant donc une proportion accrue de réticulations L-D. Cela souligne la spécificité de TtsA pour les réticulations L-D, qui sont introduites par YcbB.
L'étude a également examiné la localisation subcellulaire de Sen1395, qui, contrairement à TtsA, ne s'est pas enrichie aux pôles et a montré une distribution uniforme autour de la surface bactérienne. Cela renforce l'idée que le domaine carboxy-terminal de TtsA est essentiel pour sa localisation polaire.
La compréhension de la purification de la muramidase et de l'analyse de ses fonctions, comme illustré par la lysozyme du lait de bufflonne et la muramidase TtsA, ouvre des voies prometteuses. La lysozyme de bufflonne, avec son activité accrue, pourrait trouver des applications dans l'industrie alimentaire comme conservateur naturel ou dans le domaine pharmaceutique pour ses propriétés antibactériennes.
Concernant TtsA, l'identification du domaine responsable de la reconnaissance du substrat et de la localisation polaire est une avancée majeure dans la compréhension de la sécrétion de la toxine typhoïde. Ces découvertes pourraient mener au développement de nouvelles stratégies thérapeutiques visant à inhiber la virulence de Salmonella Typhi en perturbant ce mécanisme de sécrétion essentiel.
En outre, l'étude de la lysozyme CcLys2 chez Coridius chinensis, un insecte médicinal, met en lumière la diversité fonctionnelle des lysozymes d'insectes. CcLys2, une lysozyme de type c, a démontré une activité lytique contre les bactéries Gram-positives à pH faible, suggérant un rôle dans l'immunité innée de l'insecte. Ces recherches fournissent des données précieuses pour l'annotation fonctionnelle de protéines similaires chez d'autres insectes et pour le développement potentiel de composants médicinaux issus de C. chinensis. Elles contribuent également à une meilleure compréhension de l'origine et de l'évolution des lysozymes d'insectes.
L'analyse comparative des structures de TtsA et de ses homologues, associée aux études fonctionnelles sur des protéines chimériques, offre une base solide pour la conception rationnelle d'inhibiteurs ou de modulateurs de l'activité des muramidases, avec des implications potentielles dans la lutte contre les infections bactériennes et la compréhension des mécanismes de virulence.
tags: #purification #de #la #muramidase #analyse