L'eau, substance omniprésente et essentielle à la vie, présente une complexité thermodynamique remarquable. Sa compréhension approfondie est cruciale pour de nombreuses applications, allant des processus industriels à la conception d'appareils de chauffage efficaces. Cet article explore les propriétés thermodynamiques de l'eau, les modèles utilisés pour les décrire, et leurs implications pratiques, notamment dans le domaine des chauffe-eau thermodynamiques.
La thermodynamique s'intéresse à la capacité d'un matériau à stocker de l'énergie sous forme thermique. Pour l'eau, plusieurs propriétés clés sont à considérer :
La capacité thermique massique, anciennement appelée chaleur massique ou chaleur spécifique, est la quantité de chaleur nécessaire pour élever la température d'une unité de masse d'une substance d'un kelvin (ou degré Celsius). Elle reflète la capacité d'un matériau à accumuler de l'énergie thermique pour une masse donnée, quand sa température augmente. Son unité dans le Système International est le joule par kilogramme-kelvin (J K⁻¹ kg⁻¹).
Pour un gaz parfait monoatomique, la capacité thermique massique à volume constant ($cv$) vaut $\frac{3}{2}R$, où $R$ est la constante universelle des gaz parfaits, quelle que soit la température. La capacité thermique massique à pression constante ($cp$) est liée à la capacité thermique massique à volume constant par la relation de Mayer : $cp - cv = R$ pour un gaz parfait. La différence entre $cp$ et $cv$ est liée au travail fourni pour dilater le corps sous une pression externe.
Dans le cas des solides, la loi de Dulong et Petit est applicable à haute température. À basse température, la contribution des phonons devient prépondérante. La capacité thermique massique d'un solide peut être mesurée par des techniques telles que l'Analyse Thermodifférentielle (ATD) ou la Calorimétrie Différentielle à Balayage (DSC). Ces appareils mesurent la différence de température entre un échantillon et une référence chauffés dans un four, permettant de déterminer la capacité thermique de l'échantillon par comparaison.
Pour les liquides, à l'instar des solides, la capacité thermique dépend principalement de la température et très peu du volume ou de la pression. Cependant, l'eau présente une capacité thermique massique anormalement élevée : $c_p(\text{eau}) = 4,2 \, \text{J.K}^{-1}\text{.g}^{-1}$, ce qui correspond à une capacité thermique molaire d'environ 75 J.K⁻¹.mol⁻¹, soit trois fois celle des solides. Cette propriété confère à l'eau une grande inertie thermique, lui permettant d'absorber ou de libérer de grandes quantités de chaleur sans variation de température significative.
La mesure de la capacité thermique des liquides est souvent réalisée par calorimétrie. Un calorimètre est une enceinte adiabatique. La méthode du mélange, utilisée pour les solides, peut être adaptée. Une masse d'eau d'une capacité thermique connue est chauffée à une température initiale $T1$. Une masse d'un solide de capacité thermique inconnue, chauffé à $T2$, est ensuite introduite. Après stabilisation, la température finale $T_f$ permet de calculer la capacité thermique du solide.
Une autre méthode, privilégiée pour les liquides et les gaz, est la mesure par écoulement stationnaire. Un liquide est mis en circulation à pression constante dans un tube calorifugé. Une résistance chauffante alimentée électriquement augmente la température du fluide. Un bilan énergétique sur la portion de fluide traversant la résistance permet de déterminer la capacité thermique $c_p$.
Le coefficient de Laplace, noté $\gamma$, est le rapport entre la capacité thermique à pression constante ($cp$) et la capacité thermique à volume constant ($cv$) : $\gamma = \frac{cp}{cv}$. Pour un gaz parfait, la relation de Mayer ($cp - cv = R$) permet d'exprimer $\gamma$ en fonction du nombre de degrés de liberté d'une molécule. Par exemple, pour un gaz parfait monoatomique, $\gamma = \frac{5}{3}$, tandis que pour un gaz diatomique, $\gamma$ dépend de la température et est proche de $\frac{7}{5}$ à température ambiante.
La thermodynamique classique n'est pas en mesure de prédire les valeurs de $\gamma$. C'est la physique statistique qui permet ces prévisions, en considérant les degrés de liberté de translation, de rotation et de vibration des molécules.
Le coefficient de Laplace est déterminant dans la description des transformations adiabatiques réversibles, qui suivent les lois de Laplace : $pV^\gamma = \text{Cte}$, $T V^{\gamma-1} = \text{Cte}$, et $T^\gamma p^{1-\gamma} = \text{Cte}$. Ces lois sont appliquées dans des situations où le transfert thermique est négligeable, comme dans l'expansion rapide d'un gaz.
L'expérience de Clément-Desormes permet de déterminer $\gamma$ pour un gaz. Elle consiste à faire entrer de l'air sous pression dans un ballon, puis à le laisser s'échapper par une détente quasi réversible. En mesurant les variations de pression et de température avant et après la détente, on peut calculer $\gamma$. La mesure de la vitesse du son dans un fluide est également une méthode pour déterminer $\gamma$.
Lorsque l'on traite des mélanges, le comportement thermodynamique peut s'écarter de celui des gaz parfaits. Des modèles thermodynamiques sont développés pour prédire les propriétés des mélanges, tels que les tensions de vapeur, la solubilité des gaz, ou les équilibres liquide-vapeur et liquide-liquide.
Le modèle du gaz parfait est un idéal où les interactions intermoléculaires sont négligées. Il est utile pour des gaz à basse pression et haute température. Cependant, pour des composés chimiques en phase liquide ou vapeur, surtout à des pressions proches de la pression atmosphérique ou plus élevées, le comportement s'écarte du modèle idéal.
Pour décrire le comportement des mélanges réels, plusieurs modèles sont employés :
Modèles basés sur les coefficients d'activité : Ces modèles incorporent des paramètres qui corrigent les écarts par rapport à l'idéalité. Ils sont particulièrement utiles pour les mélanges liquides. Des exemples incluent le modèle de Wilson et le modèle UNIQUAC (Universal Quasi Chemical). Ces modèles sont souvent ajustés sur des données expérimentales par des calculs de régression pour déterminer les paramètres spécifiques à chaque système et à chaque modèle.
Modèles d'équations d'état : Ces modèles décrivent la relation entre pression, volume et température pour des fluides réels. Ils sont applicables aux phases liquide et vapeur, et permettent de calculer les propriétés d'équilibre liquide-vapeur.
Le choix du modèle thermodynamique dépend de la précision requise, de la nature des composés chimiques impliqués, et des conditions de température et de pression. L'industrie chimique consacre des modèles particuliers à des systèmes spécifiques en raison de leur importance économique ou de leur comportement complexe.
La compréhension des propriétés thermodynamiques de l'eau est fondamentale pour le développement de technologies économes en énergie, comme les chauffe-eau thermodynamiques.
Un chauffe-eau thermodynamique, également appelé ballon thermodynamique ou cumulus thermodynamique, combine un ballon de stockage d'eau chaude et une pompe à chaleur intégrée. Il utilise les calories présentes dans l'air ambiant pour chauffer l'eau. Le principe repose sur le cycle de la pompe à chaleur :
Ce système permet de produire jusqu'à trois ou quatre fois plus d'énergie thermique qu'il n'en consomme en électricité, se traduisant par des économies d'énergie allant jusqu'à 70 % par rapport à un chauffe-eau électrique classique. Le Coefficient de Performance (COP) d'une pompe à chaleur évalue cette efficacité. Un COP de 3,1 signifie qu'1 kWh d'électricité consommé produit environ 3 kWh de chaleur.
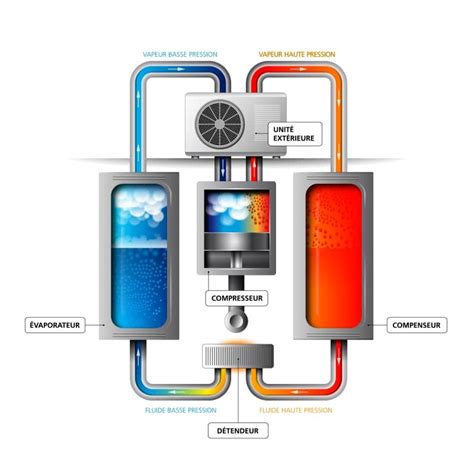
Il existe deux configurations principales :
Les chauffe-eau thermodynamiques sont compatibles avec les énergies renouvelables, notamment l'autoproduction photovoltaïque, et peuvent être couplés à des systèmes de ventilation mécanique contrôlée (VMC) pour récupérer les calories de l'air extrait. Ils représentent une alternative écologique et économique, réduisant la facture énergétique et l'empreinte carbone, sans recours aux combustibles fossiles. L'installation est rapide et facile, et le niveau sonore est comparable à celui d'un réfrigérateur (40-50 décibels).

Le choix de la capacité du ballon dépend de la taille du foyer (de 180 à 300 litres pour 3 à 5 personnes). Le coût d'un chauffe-eau thermodynamique, installation comprise, varie généralement entre 2 000 et 5 000 €, en fonction de la capacité, du type de chauffe (air ambiant, air extérieur, air extrait) et de la configuration. Le retour sur investissement est estimé entre 4 et 6 ans grâce aux économies d'énergie réalisées.
Un entretien régulier, comprenant la vérification de l'échangeur, de l'anode de protection contre la corrosion et du groupe de sécurité, garantit le maintien des performances et la durée de vie de l'appareil, qui peut atteindre quinze ans.
La capacité thermique massique élevée de l'eau est un facteur clé de l'efficacité des chauffe-eau thermodynamiques. Cette propriété permet au système de stocker une grande quantité d'énergie thermique, assurant un approvisionnement confortable en eau chaude sanitaire. Par rapport à d'autres liquides, l'eau demande une quantité d'énergie plus importante pour augmenter sa température, ce qui, dans le contexte d'un cycle thermodynamique, se traduit par une capacité de stockage thermique accrue.
La thermodynamique de l'eau, bien que complexe, est la clé de nombreuses avancées technologiques. De la prédiction fine du comportement des mélanges chimiques à la conception d'appareils de chauffage économes en énergie comme les chauffe-eau thermodynamiques, la maîtrise de ses propriétés est indispensable. Les modèles thermodynamiques, qu'ils soient simples ou sophistiqués, permettent de modéliser avec précision ces comportements, ouvrant la voie à des solutions plus durables et efficaces.
tags: #gamma #eau #thermodynamique