La thermodynamique, branche fondamentale de la physique, étudie les échanges d'énergie sous forme de chaleur et de travail, ainsi que leurs transformations. Le premier principe de la thermodynamique, également connu sous le nom de principe de conservation de l'énergie, établit que l'énergie d'un système isolé reste constante. Ce principe est la pierre angulaire de nombreux phénomènes physiques et trouve des applications concrètes dans diverses situations, allant du fonctionnement des centrales électriques à l'isolation thermique des bâtiments. Cette exploration se concentrera sur des exercices corrigés illustrant l'application de ces principes.
Un concept clé en thermodynamique est l'équilibre thermique. Lorsque deux objets de températures différentes sont mis en contact, l'énergie thermique se transfère spontanément de l'objet le plus chaud vers l'objet le plus froid jusqu'à ce qu'ils atteignent la même température. Ce processus est régi par la loi du refroidissement de Newton, qui stipule que le taux de transfert de chaleur est proportionnel à la différence de température entre l'objet et son environnement.
Considérons un exemple concret : si un thermomètre placé dans une pièce indique depuis longtemps $\pu{18 °C}$, cela signifie que l'air de la pièce a atteint cette température. Dans ce cas, les objets en marbre et en bois présents dans la pièce, s'ils ont été dans cet environnement pendant une durée suffisante, auront également atteint cette température d'équilibre de $\pu{18 °C}$. La température du corps humain, qui est d'environ $\pu{37 °C}$, est supérieure à celle de la pièce. Si une personne se trouve dans cette pièce, il y aura un transfert d'énergie thermique de son corps vers l'air ambiant, jusqu'à ce que la température corporelle soit maintenue par les mécanismes de régulation du corps.
Un thermostat est défini comme un système de capacité thermique infinie. Cela signifie qu'il peut absorber ou céder une quantité illimitée de chaleur sans que sa propre température ne change. Il agit comme un réservoir de température constante, maintenant ainsi la température d'un système donné à une valeur prédéfinie.
Prenons le cas de Joachim qui a oublié sa canette de soda, initialement à $\pu{5 °C}$, en plein soleil. La température ambiante est de $\pu{25 °C}$. La canette en aluminium, de masse $m_{\ce{Al}} = \pu{14 g}$, va absorber de l'énergie du soleil et de l'air ambiant. Même si la température ambiante est de $\pu{25 °C}$, le rayonnement solaire peut chauffer la canette à une température supérieure. Lorsque la température de la canette atteint l'équilibre avec son environnement (la température ambiante et le rayonnement solaire), les transferts d'énergie n'ont pas nécessairement cessé. Il y a toujours des échanges d'énergie, mais le bilan net est nul : la quantité d'énergie absorbée est égale à la quantité d'énergie cédée.
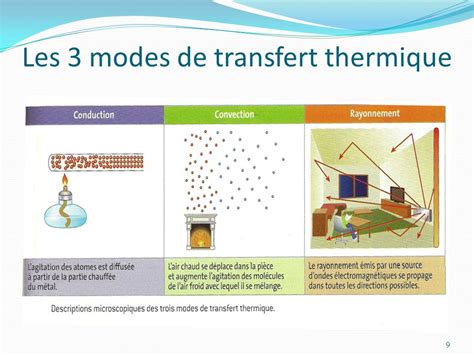
La calorimétrie est l'ensemble des techniques de mesure de transferts thermiques. Elle est essentielle pour déterminer des grandeurs telles que les énergies de changement d'état (fusion, vaporisation) et les capacités thermiques des matériaux.
Un calorimètre à vase de Dewar est un instrument sophistiqué conçu pour minimiser les échanges de chaleur avec l'environnement extérieur, permettant ainsi des mesures précises. Il se compose d'un récipient métallique muni d'un couvercle et d'un système d'agitation. À l'intérieur, on trouve un vase à double paroi en verre, dont les surfaces internes sont argentées et séparées par du vide. L'argenture réfléchit le rayonnement thermique, tandis que le vide constitue une excellente barrière isolante contre les transferts de chaleur par conduction et convection.
Considérons une expérience visant à déterminer la capacité thermique massique $c2$ du cuivre solide. On place une masse $m1 = \pu{80,1 g}$ d'eau liquide dans un calorimètre. Dans une étuve, un bloc de cuivre solide de masse $m2 = \pu{62,3 g}$ est chauffé à une température $T2 = \pu{75,0 °C}$. Ce bloc est ensuite rapidement transféré dans l'eau du calorimètre, et le système est fermé.
Pour établir le bilan énergétique, nous considérons que le système {eau + bloc de cuivre} est isolé thermiquement de son environnement grâce au calorimètre. L'énergie thermique cédée par le bloc de cuivre chaud est égale à l'énergie thermique absorbée par l'eau plus l'énergie thermique absorbée par le calorimètre lui-même (si sa capacité thermique n'est pas négligeable). Si l'on néglige la capacité thermique du calorimètre et les pertes de chaleur, le bilan s'écrit :
$Q{\text{cuivre}} + Q{\text{eau}} = 0$
$m2 c2 (Tf - T2) + m1 c1 (Tf - T1) = 0$
où $Tf$ est la température finale d'équilibre, $c1$ est la capacité thermique massique de l'eau, et $T_1$ est la température initiale de l'eau.
En déduire l'expression de la capacité thermique massique $c_2$ du cuivre :
$m2 c2 (Tf - T2) = - m1 c1 (Tf - T1)$
$c2 = \frac{- m1 c1 (Tf - T1)}{m2 (Tf - T2)} = \frac{m1 c1 (T1 - Tf)}{m2 (T2 - T_f)}$
Pour calculer $c2$, il faut connaître la température finale d'équilibre $Tf$. Supposons que la température finale mesurée soit $Tf = \pu{20,0 °C}$ et que la capacité thermique massique de l'eau soit $c1 = \pu{4,18 J.g-1.°C-1}$.
$c_2 = \frac{\pu{80,1 g} \times \pu{4,18 J.g-1.°C-1} \times (\pu{20,0 °C} - \pu{20,0 °C})}{\pu{62,3 g} \times (\pu{75,0 °C} - \pu{20,0 °C})} = \frac{\pu{80,1 g} \times \pu{4,18 J.g-1.°C-1} \times \pu{0 °C}}{\pu{62,3 g} \times \pu{55,0 °C}}$
Il semble y avoir une erreur dans l'énoncé ou dans ma compréhension car avec $T1 = \pu{20 °C}$ et $Tf = \pu{20 °C}$, le cuivre n'aurait pas cédé de chaleur. Reformulons avec une température initiale de l'eau $T1 = \pu{18,0 °C}$ et une température finale d'équilibre $Tf = \pu{21,0 °C}$.
$c_2 = \frac{\pu{80,1 g} \times \pu{4,18 J.g-1.°C-1} \times (\pu{18,0 °C} - \pu{21,0 °C})}{\pu{62,3 g} \times (\pu{21,0 °C} - \pu{75,0 °C})} = \frac{\pu{80,1 g} \times \pu{4,18 J.g-1.°C-1} \times (-\pu{3,0 °C})}{\pu{62,3 g} \times (-\pu{54,0 °C})}$
$c_2 = \frac{\pu{1005,7 J}}{\pu{3364,2 J.°C-1}} \approx \pu{0,30 J.g-1.°C-1}$
Cette valeur calculée est différente de la valeur lue dans les tables thermodynamiques, qui est $\pu{0,390 J.g-1.°C-1}$.
Les sources d'erreur lors de la détermination de la capacité thermique massique sont multiples :
Dans une autre expérience de calorimétrie, un calorimètre contient $m1 = \pu{95 g}$ d’eau à $\theta1 = \pu{20 °C}$. On ajoute $m2 = \pu{71 g}$ d’eau à $\theta2 = \pu{50 °C}$. Le même calorimètre contient maintenant $m’1 = \pu{100 g}$ d’eau à $\theta’1 = \pu{15 °C}$. On y plonge un échantillon métallique de masse $m = \pu{25 g}$ sortant d’une étuve à $\theta’_2 = \pu{95 °C}$. La température d’équilibre est $\theta = \pu{16,7 °C}$.
Le bilan énergétique pour ce système {eau + échantillon métallique} est :
$Q{\text{eau initiale}} + Q{\text{eau ajoutée}} + Q_{\text{métal}} = 0$ (en négligeant la capacité thermique du calorimètre et les pertes).
Ici, les températures initiales de l'eau sont différentes, il faut donc les considérer séparément avant le mélange final. Cependant, l'énoncé semble présenter deux scénarios distincts pour le calorimètre, ce qui est une source de confusion. Reformulons l'énoncé pour qu'il soit cohérent : Un calorimètre contient une masse d'eau initiale. On y plonge un échantillon métallique chauffé.
Supposons que le calorimètre contienne initialement $m1 = \pu{100 g}$ d’eau à $\theta1 = \pu{15 °C}$. On y plonge un échantillon métallique de masse $m = \pu{25 g}$ sortant d’une étuve à $\theta_2 = \pu{95 °C}$. La température d’équilibre est $\theta = \pu{16,7 °C}$.
Le bilan énergétique est :$Q{\text{eau}} + Q{\text{métal}} = 0$$m1 c{\text{eau}} (\theta - \theta1) + m c{\text{métal}} (\theta - \theta_2) = 0$
L'objectif est de trouver la capacité thermique massique du métal, $c{\text{métal}}$.$\pu{100 g} \times \pu{4,18 J.g-1.°C-1} \times (\pu{16,7 °C} - \pu{15 °C}) + \pu{25 g} \times c{\text{métal}} \times (\pu{16,7 °C} - \pu{95 °C}) = 0$
$\pu{100} \times \pu{4,18} \times \pu{1,7} + \pu{25} \times c_{\text{métal}} \times (-\pu{78,3}) = 0$
$\pu{710,6} + \pu{25} \times c{\text{métal}} \times (-\pu{78,3}) = 0$$\pu{710,6} = \pu{1957,5} \times c{\text{métal}}$$c_{\text{métal}} = \frac{\pu{710,6}}{\pu{1957,5}} \approx \pu{0,363 J.g-1.°C-1}$
Ce résultat nous donne une idée de la capacité thermique du métal.
Les principes de la thermodynamique sont omniprésents. Les fours à micro-ondes, par exemple, utilisent des ondes électromagnétiques qui sont absorbées par les molécules d'eau contenues dans les aliments. Cette absorption provoque une oscillation des molécules d'eau, générant ainsi de la chaleur et augmentant la température des aliments. La puissance d'un four, comme $\pu{750 W}$, indique le taux auquel il délivre de l'énergie. Chauffer $\pu{500 g}$ d'eau avec ce four implique un transfert d'énergie qui augmente la température de l'eau selon la relation $Q = mc\Delta T$.
L'isolation thermique est un autre domaine d'application crucial. L'utilisation de matériaux comme la laine de verre pour isoler la toiture d'une maison vise à réduire les transferts de chaleur entre l'intérieur et l'extérieur. La conductivité thermique $\lambda$ d'un matériau quantifie sa capacité à conduire la chaleur. Une faible valeur de $\lambda$ indique un bon isolant. Si l'on soumet une face de la laine de verre à $TA = \pu{10 °C}$ et l'autre face à $TB = \pu{30 °C}$, le flux de chaleur à travers le matériau dépendra de son épaisseur et de sa conductivité thermique.

Dans le contexte des centrales électronucléaires, une grande partie de l'énergie libérée par la fission de l'uranium n'est pas convertie en énergie électrique. Cette énergie thermique résiduelle doit être évacuée par un circuit d'eau de refroidissement. Ce circuit est vital pour la sécurité, car une défaillance de l'alimentation en eau peut entraîner une augmentation de température menant à la fusion du cœur du réacteur. Le cœur du réacteur fournit une énergie thermique $Q$ à la centrale. L'eau du circuit de refroidissement, initialement à $T = \pu{16 °C}$, reçoit une énergie thermique $Q’$ de la centrale, et le travail électrique fourni au réseau est $W$. Ces éléments sont liés par le premier principe de la thermodynamique appliqué à la centrale en tant que machine thermique.
Les pompes à chaleur (PAC) sont encouragées pour le chauffage des habitations. Elles fonctionnent en utilisant une quantité de travail $W$ (fourni par une prise de courant) pour transférer de la chaleur d'une source froide (l'extérieur) vers une source chaude (l'intérieur de l'habitation). Ce processus est rendu possible par un cycle thermodynamique réversible.
Le vitrage d'une fenêtre d'immeuble, d'une surface $S = \pu{2,4 m2}$, peut être composé de double vitrage pour améliorer l'isolation. La représentation graphique de l'évolution de la température dans un double vitrage en fonction de la distance $x$ permet d'analyser les transferts de chaleur. La température de la face intérieure de la vitre en contact avec l'air extérieur à l'immeuble dépendra de la température intérieure de l'immeuble et de la résistance thermique du double vitrage. La résistance thermique de $\pu{16 mm}$ d'air, par exemple, peut être calculée à partir de la conductivité thermique de l'air et de l'épaisseur. Comparer cette résistance à celle d'un mur en béton de $\pu{20 cm}$ d'épaisseur permet d'évaluer l'efficacité de l'isolation.
Le premier principe de la thermodynamique s'applique également aux transformations d'énergie mécanique en énergie thermique. Imaginons une bille métallique lancée vers le haut avec une vitesse $v_0$ dans le champ de pesanteur $\vec{g}$. Au fur et à mesure qu'elle monte, son énergie cinétique diminue et se transforme en énergie potentielle de pesanteur. Lorsqu'elle atteint son apogée, toute son énergie cinétique initiale s'est transformée en énergie potentielle. Si l'on considère les frottements de l'air, une partie de cette énergie mécanique est dissipée sous forme de chaleur.
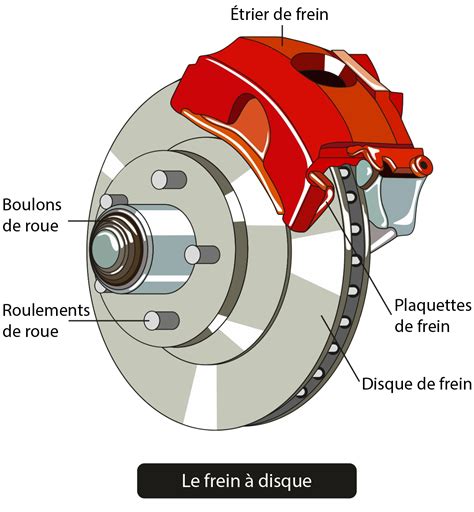
Une auto de masse $M = \pu{836 kg}$ roulant à la vitesse $v = \pu{20 m.s-1}$ (72 km/h) et s'arrêtant brusquement à l'aide de ses freins à disques est un exemple frappant de conversion d'énergie cinétique en énergie thermique. Le système {voiture + environnement} est considéré comme isolé pendant le freinage, ce qui signifie que les échanges thermiques avec l'environnement sont négligeables sur la courte durée du freinage. L'énergie cinétique initiale de la voiture $E_c = \frac{1}{2} Mv^2$ est entièrement dissipée sous forme de chaleur au niveau des freins, augmentant ainsi leur température. La masse des disques $m$ intervient dans le calcul de l'élévation de température des freins.
Considérons un cylindre fermé horizontal divisé en deux compartiments $A$ et $B$ de même volume $V0$ par un piston coulissant librement. Chaque compartiment contient une mole de gaz parfait à la pression $P0$ et à la température $T_0$. Le piston et les parois latérales du cylindre sont athermanes, c'est-à-dire qu'ils ne transmettent pas d'énergie thermique. Si une transformation se produit dans l'un des compartiments, par exemple si le compartiment $A$ est chauffé, le gaz se dilate, pousse le piston et comprime le gaz dans le compartiment $B$.
Si le piston est initialement en équilibre, la pression dans les deux compartiments est égale. Si un travail est effectué sur le gaz dans le compartiment $A$ (par exemple, par compression) ou si de la chaleur est ajoutée, son énergie interne peut varier. Pour un gaz parfait, la variation d'énergie interne $\Delta U$ ne dépend que de la variation de température $\Delta T$ et est donnée par $\Delta U = n Cv \Delta T$, où $n$ est le nombre de moles et $Cv$ est la capacité thermique molaire à volume constant. La variation d'énergie interne du gaz à l'intérieur de $A$ sera différente de celle de $B$ si les transformations subies par les deux gaz ne sont pas identiques.
Le programme de physique-chimie en Terminale prépare les élèves aux épreuves du baccalauréat et à l'accès aux études supérieures. L'assimilation des concepts de thermodynamique est donc essentielle.
L'immersion d'un dipôle ohmique de capacité thermique négligeable dans l'eau d'un calorimètre, en régime permanent, signifie que la température de l'eau et du dipôle ne varie plus au cours du temps. Si un courant électrique traverse le dipôle, il dissipe de l'énergie sous forme de chaleur, ce qui doit être compensé par des échanges thermiques avec l'environnement pour maintenir une température constante.
L'effet de l'altitude sur la respiration est un exemple d'application des gaz. À chaque inspiration, un alpiniste emplit ses poumons d'un volume d'air donné, mais à haute altitude, la pression de l'air est plus faible. Par conséquent, la masse d'air, et donc la quantité de dioxygène inspirée, est inférieure.
La comparaison de la résistance thermique d'un double vitrage avec celle d'une fenêtre simple vitrage met en évidence l'efficacité de l'isolation. Une valeur de résistance thermique environ 13 fois plus grande pour le double vitrage indique une réduction significative des pertes de chaleur.
L'utilisation de simulateurs du bac et la pratique régulière d'exercices sont recommandées pour maîtriser ces concepts.
tags: #exercices #thermodynamique #premier #corrige