La distillation est un procédé fondamental dans l'industrie chimique, permettant la séparation de mélanges liquides en fonction de leurs points d'ébullition. L'efficacité de ce processus, et par conséquent le nombre d'étages théoriques nécessaires pour atteindre une pureté désirée, est fortement influencée par plusieurs paramètres, dont la pression de fonctionnement. Cet article explore l'impact de la pression sur le calcul thermodynamique des distillateurs, en se concentrant sur des exercices pratiques impliquant la séparation de mélanges méthanol-eau et éthanol-eau. Nous examinerons comment les variations de pression affectent le nombre d'étages requis et aborderons la conception d'une colonne de distillation pour une séparation spécifique d'éthanol-eau, en tenant compte des limitations imposées par les azéotropes.
La séparation d'un mélange méthanol-eau est un cas d'étude classique pour comprendre les principes de la distillation. Dans un scénario donné, nous cherchons à distiller un mélange méthanol-eau à 40% en fraction molaire de méthanol. L'objectif est d'obtenir du méthanol pur à 98% en tête de colonne et de l'eau pure à 97% en pied. Le taux de reflux est fixé à 1,5. La question centrale est d'étudier l'effet de la pression sur le nombre d'étages nécessaires pour réaliser cette séparation.
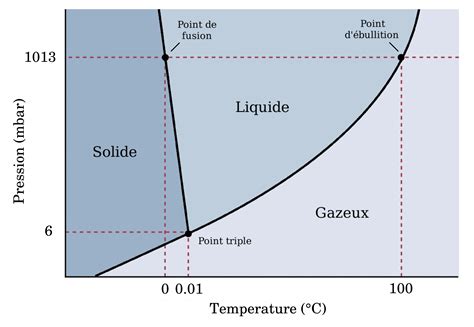
Pour étudier cet effet, il est judicieux de faire varier la pression sur une plage significative, par exemple entre 0,1 et 20 bars. À chaque pression, le calcul du nombre d'étages théoriques peut être effectué en utilisant les diagrammes d'équilibre liquide-vapeur spécifiques au système méthanol-eau à cette pression. Les diagrammes d'équilibre, qui représentent les fractions molaires des composants dans la phase liquide et la phase vapeur à l'équilibre, sont cruciaux pour ce type de calcul. Ils sont généralement obtenus à partir de données expérimentales ou de modèles thermodynamiques fiables.
À basse pression, les différences de volatilité relative entre les composants sont généralement plus marquées, ce qui peut potentiellement réduire le nombre d'étages requis. Inversement, à haute pression, les volatilités relatives tendent à se rapprocher, nécessitant ainsi un plus grand nombre d'étages pour atteindre la même pureté. Cette tendance est souvent observée pour de nombreux mélanges binaires. Cependant, il est important de noter que la forme des courbes d'équilibre peut varier avec la pression, et dans certains cas, des effets non linéaires peuvent apparaître.
Le calcul du nombre d'étages théoriques est typiquement réalisé à l'aide de la méthode de McCabe-Thiele, qui utilise graphiquement les courbes d'équilibre et les droites d'opération (droite de reflux et droite de produits). La droite de reflux, dont la pente dépend du taux de reflux et de la composition du distillat, relie la composition du distillat à la composition du mélange entrant dans la colonne. La droite de produits relie la composition du résidu à la composition du mélange entrant. L'intersection de ces droites détermine la composition du mélange entrant, et le nombre d'étages est ensuite obtenu en traçant une série d'étages entre la courbe d'équilibre et la droite de produits, puis entre la courbe d'équilibre et la droite de reflux.
Lorsque la pression augmente, les points d'ébullition des deux composants augmentent. La volatilité relative, définie comme le rapport des coefficients d'activité des composants, est un indicateur clé de la facilité de séparation. Pour le système méthanol-eau, la volatilité relative diminue généralement avec l'augmentation de la pression. Une volatilité relative plus faible signifie que la vapeur formée est moins enrichie en composant le plus volatil (le méthanol dans ce cas) par rapport au liquide. Par conséquent, pour atteindre la même pureté de distillat et de résidu, un plus grand nombre d'étages sera nécessaire à des pressions plus élevées. L'étude de l'effet de la pression impliquerait donc de tracer les diagrammes d'équilibre à différentes pressions, puis d'appliquer la méthode de McCabe-Thiele pour chaque cas et de comparer les nombres d'étages obtenus.
Il est également essentiel de considérer les implications pratiques. Opérer à basse pression peut nécessiter des équipements sous vide, ce qui peut être coûteux en termes d'investissement et de consommation d'énergie pour la création et le maintien du vide. À l'inverse, opérer à haute pression peut nécessiter des équipements plus robustes et peut augmenter les risques liés à la sécurité. Le choix de la pression de fonctionnement optimale est donc un compromis entre l'efficacité de la séparation, les coûts d'investissement, les coûts d'exploitation et les considérations de sécurité. La conception d'une colonne de distillation ne se limite pas au nombre d'étages théoriques ; elle inclut également le choix du type de plateaux ou de garnissage, le diamètre de la colonne, et la gestion des flux thermiques (apport de chaleur au rebouilleur et reflux de condensat).
Passons maintenant à un autre défi de séparation : obtenir de l'éthanol pur à 90% en fraction molaire à partir d'un mélange à 15%. Un critère supplémentaire est imposé : une fraction molaire de 1% d'éthanol dans le résidu est requise, assurant ainsi une bonne récupération de l'éthanol purifié. La difficulté majeure dans la séparation de l'éthanol et de l'eau réside dans la présence d'un azéotrope à pression atmosphérique.
Un azéotrope est un mélange de deux ou plusieurs liquides dont le comportement d'ébullition est tel que la phase vapeur a la même composition que la phase liquide. Pour le mélange binaire éthanol (A) - eau (B) sous pression atmosphérique, un azéotrope est observé à une composition de (xA = yA = 0,895) et à une température de 351,2 K. Cela signifie qu'une distillation conventionnelle ne peut pas séparer ce mélange au-delà de la composition azéotropique. Si l'on tente de distiller un mélange dont la composition est inférieure ou supérieure à celle de l'azéotrope, le distillat ou le résidu (selon le cas) atteindra la composition azéotropique et ne pourra pas être purifié davantage par distillation simple.
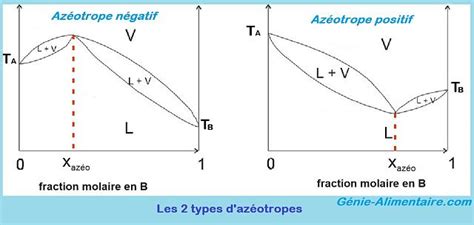
Dans le cas présent, où nous partons d'un mélange à 15% d'éthanol et visons une pureté de 90%, la distillation à pression atmosphérique est donc impossible, puisqu'il faudrait "traverser" l'azéotrope. Pour surmonter cette limitation, plusieurs stratégies peuvent être employées :
Distillation à pression différente : L'azéotrope n'est pas une caractéristique fixe de tous les systèmes binaires ; sa composition et sa température varient avec la pression. En opérant à une pression différente de la pression atmosphérique, il est possible de déplacer la composition de l'azéotrope. Si l'on peut opérer à une pression où l'azéotrope se forme à une composition supérieure à 90% d'éthanol, alors la séparation devient possible par distillation conventionnelle. Alternativement, si l'azéotrope se déplace vers une composition inférieure, il pourrait être possible de séparer l'éthanol jusqu'à une pureté supérieure à 90% dans le distillat, mais la récupération de l'eau pure deviendrait problématique. Il est donc nécessaire de consulter les diagrammes d'équilibre éthanol-eau à différentes pressions pour identifier une plage de pression appropriée. Par exemple, à des pressions plus élevées, l'azéotrope éthanol-eau se déplace vers des compositions plus riches en éthanol.
Extraction par solvant : Cette méthode implique l'ajout d'un troisième composant (solvant) qui modifie les coefficients d'activité de l'éthanol et de l'eau, rompant ainsi l'azéotrope. Le solvant est choisi de manière à former des phases liquides non miscibles avec le mélange éthanol-eau, permettant une séparation sélective. Après la séparation initiale, le solvant doit être séparé de l'éthanol ou de l'eau dans des étapes de distillation ultérieures.
Distillation azéotropique : Similaire à l'extraction par solvant, cette technique utilise un agent entraîneur qui forme un nouvel azéotrope avec l'un des composants (généralement l'eau) et qui est plus facile à séparer. Par exemple, le cyclohexane peut être utilisé comme agent entraîneur pour former un azéotrope hétérogène avec l'eau, permettant d'éliminer l'eau sous forme d'azéotrope et d'obtenir de l'éthanol anhydre.
Distillation extractive : Dans ce cas, un solvant à point d'ébullition élevé est ajouté au mélange. Ce solvant modifie la volatilité relative des composants du mélange d'origine, rendant possible la séparation par distillation. Le solvant, ayant un point d'ébullition élevé, reste dans le résidu de la colonne principale et est ensuite séparé dans une colonne secondaire.
Pervaporation : Cette technique utilise une membrane semi-perméable qui permet à un composant de passer préférentiellement à travers elle, créant ainsi une séparation. La pervaporisation est particulièrement efficace pour la séparation de mélanges azéotropiques et pour la déshydratation des alcools.
Pour notre exercice, nous devons déterminer une colonne permettant la séparation visée. Si nous choisissons de travailler à une pression différente, il faudrait d'abord identifier cette pression optimale. Par exemple, si à une pression donnée, l'azéotrope se forme à 95% d'éthanol, alors une colonne de distillation conventionnelle pourrait être conçue. Le calcul du nombre d'étages serait alors similaire à celui présenté précédemment, mais en utilisant les courbes d'équilibre à cette pression spécifique. La droite de reflux et la droite de produits seraient tracées en fonction des compositions désirées (distillat à 90%, résidu à 1% d'éthanol) et des conditions opératoires (taux de reflux, composition du mélange entrant).
Si une pression alternative ne permet pas de surmonter l'azéotrope, alors d'autres méthodes comme la distillation azéotropique ou extractive devraient être envisagées. La conception impliquerait alors un schéma de procédé plus complexe, potentiellement avec plusieurs colonnes. Par exemple, dans une distillation azéotropique avec un agent entraîneur, une première colonne pourrait être conçue pour séparer l'agent entraîneur formant un azéotrope avec l'eau du mélange. Le distillat de cette colonne serait cet azéotrope, qui serait ensuite traité dans une seconde étape (par exemple, décantation si l'azéotrope est hétérogène) pour récupérer l'agent entraîneur et l'eau. L'éthanol purifié sortirait du fond de la première colonne.
Il est également crucial de considérer les implications de la fraction molaire imposée dans le résidu (1% d'éthanol). Atteindre une très faible concentration de produit désiré dans le résidu nécessite généralement un nombre d'étages plus élevé dans la section de la colonne correspondant à la zone de produits du résidu. La conception de la colonne doit donc équilibrer l'atteinte de la pureté du distillat avec la récupération souhaitée dans le résidu, tout en tenant compte des contraintes économiques et techniques. La détermination du nombre d'étages minimum est une étape clé, mais la sélection d'un taux de reflux approprié est également importante. Un taux de reflux plus élevé réduit le nombre d'étages mais augmente la consommation d'énergie (plus de condensat à refroidir et à re-vaporiser).
En résumé, la conception d'une colonne de distillation pour séparer l'éthanol et l'eau au-delà de leur azéotrope nécessite une compréhension approfondie des diagrammes d'équilibre à différentes pressions et potentiellement l'application de techniques de séparation avancées. Le choix de la méthode dépendra des contraintes spécifiques du procédé, des coûts et de la pureté désirée, en veillant à l'efficacité de la récupération du produit.
tags: #exercice #calcul #thermodynamique #dans #un #distillateur