En chimie organique, la capacité d'une réaction à produire un composé spécifique parmi plusieurs possibilités est d'une importance capitale. Cette sélectivité est souvent le fruit d'un équilibre délicat entre la vitesse de formation des produits et leur stabilité intrinsèque. Au cœur de nombreuses transformations impliquant des composés carbonylés, les énolates jouent un rôle central, et leur formation, qu'elle soit cinétique ou thermodynamique, dicte le paysage réactionnel. Comprendre ces deux régimes est essentiel pour anticiper et contrôler les résultats d'une réaction, particulièrement dans des contextes tels que les réactions d'aldolisation ou les additions sur des diènes conjugués.
Lorsqu'une cétone asymétrique est traitée par une base, la déprotonation peut s'opérer sur l'un des carbones alpha adjacents au groupe carbonyle, conduisant à la formation d'énolates distincts. Cette distinction est fondamentale :
L'énolate cinétique résulte de la déprotonation du proton alpha le plus accessible stériquement. Sa formation est rapide, dictée par une énergie d'activation plus faible. Les conditions favorisant le contrôle cinétique incluent l'utilisation de bases fortes et encombrées, ainsi que des températures basses. Ces conditions visent à minimiser la probabilité de réactions secondaires, y compris l'échange de protons, qui pourraient mener à l'énolate thermodynamique. En pratique, l'utilisation de bases fortement non nucléophiles et encombrées, telles que le LDA (diisopropylamidure de lithium), dans des solvants aprotiques à basse température, est une stratégie courante pour isoler l'énolate cinétique. La différence significative en pKb entre la base forte utilisée et l'énolate formé rend la déprotonation pratiquement irréversible sous ces conditions.
L'énolate thermodynamique, quant à lui, est le produit le plus stable, généralement celui où le groupe énolate est le plus substitué. Sa formation est plus lente, car elle implique une énergie d'activation plus élevée. Pour favoriser l'énolate thermodynamique, des conditions permettant l'équilibration sont nécessaires. Cela implique l'utilisation de bases plus faibles qui permettent un équilibre entre la cétone de départ et l'énolate, ou l'emploi de temps de réaction plus longs et/ou de températures plus élevées. Dans ce cas, l'énolate cinétique, une fois formé, peut s'isomériser en l'énolate thermodynamique plus stable par un échange de protons réversible avec la cétone non déprotonée. Le contrôle thermodynamique est atteint lorsque le système a eu le temps d'atteindre l'équilibre, favorisant ainsi l'espèce la plus stable.
La distinction entre ces deux régimes est cruciale, car elle impacte directement la sélectivité des réactions subséquentes. Par exemple, dans une réaction d'aldolisation, l'énolate réagira avec un électrophile, et le produit formé dépendra de la nature de l'énolate utilisé. Si l'on souhaite obtenir un produit spécifique, il est impératif de contrôler les conditions pour favoriser soit l'énolate cinétique, soit l'énolate thermodynamique.
La question de savoir quel énolate "requiert des conditions équilibrantes" pointe directement vers la définition du contrôle thermodynamique. En effet, le contrôle thermodynamique ne peut s'exercer que si la réaction est réversible et permet un échange entre les différentes espèces formées.
Réversibilité et Équilibration : Le contrôle thermodynamique est intrinsèquement lié à la capacité d'un système à atteindre un état d'équilibre. Pour qu'un énolate thermodynamique soit favorisé, il faut qu'il soit possible de passer de l'énolate cinétique à l'énolate thermodynamique. Ce processus d'équilibration est souvent réalisé par un échange de protons, où l'énolate cinétique, par exemple, peut réagir avec une molécule de cétone non déprotonée, transférant un proton et formant ainsi l'énolate thermodynamique. Si une base beaucoup moins forte est utilisée, la déprotonation sera incomplète, et il y aura un équilibre entre les réactifs et les produits. Dans ce cas, un contrôle thermodynamique s'imposera, bien que la réaction puisse rester incomplète à moins que l'énolate ne soit piégé.
Temps et Température : Les conditions de réaction jouent un rôle déterminant dans l'atteinte de cet équilibre. Les temps de réaction prolongés favorisent le contrôle thermodynamique, car ils donnent au système le temps nécessaire pour s'ajuster vers la configuration la plus stable. De même, des températures plus élevées accélèrent les processus d'équilibration, permettant à l'énolate thermodynamique de se former et de dominer. À l'inverse, des températures plus basses et des temps de réaction courts tendent à piéger l'énolate cinétique, favorisant ainsi le contrôle cinétique.
L'importance du Mécanisme d'Équilibration : La possibilité d'un mécanisme d'équilibration est la pierre angulaire du contrôle thermodynamique. Si le chemin réactionnel est tel que l'énolate cinétique, bien que formé plus rapidement, passe par un état de transition plus élevé et est donc moins stable, et qu'il existe un chemin réversible pour se convertir en un énolate plus stable (formé via un état de transition plus bas), alors le contrôle thermodynamique devient possible. Le système évoluera vers le produit le plus stable une fois que l'équilibre sera atteint.
Il est important de noter que sous un régime purement cinétique, la distribution des produits dépend uniquement des vitesses de formation, lesquelles sont déterminées par les énergies d'activation (Ea ou ΔG‡). Sous un régime purement thermodynamique, l'équilibre est atteint, et la distribution des produits est fonction des stabilités thermodynamiques (G°). En pratique, un contrôle purement cinétique est difficile à atteindre car l'équilibration tend à s'amorcer avant même la consommation complète des réactifs.
Les réactions d'aldolisation, impliquant la condensation d'un composé carbonylé avec un autre en présence d'une base ou d'un acide, illustrent parfaitement les concepts de contrôle cinétique et thermodynamique. Prenons l'exemple de la 2,4-hexanedione, une dicétone asymétrique, dans le contexte d'une réaction d'aldolisation.
La 2,4-hexanedione possède trois positions alpha potentiellement déprotonables : les protons en C1, C3 et C5. La déprotonation peut donc mener à différents énolates. La complexité s'accroît lorsque cette dicétone réagit avec un aldéhyde.
Condensation de la Dicétone sur l'Aldéhyde : La dicétone peut se condenser sur l'aldéhyde de plusieurs manières. Les trois positions adjacentes aux carbonyles de la dicétone (C1, C3 et C5) peuvent être déprotonées pour former des énolates qui attaquent ensuite le carbone électrophile de l'aldéhyde. De plus, la dicétone elle-même peut agir comme électrophile, et les énolates formés à partir d'une autre molécule de dicétone peuvent l'attaquer.
Attaque de l'Énolate de l'Aldéhyde : La correction de l'examen mentionne également l'attaque de l'énolate de l'aldéhyde sur l'une des fonctions carbonylées de la dicétone. Ceci ajoute encore une couche de complexité, car l'aldéhyde peut lui-même former un énolate qui réagit avec les carbonyles de la dicétone.
Auto-condensation : Une possibilité souvent considérée est l'auto-condensation de l'aldéhyde sur lui-même. Si l'on forme l'énolate de l'aldéhyde, il réagira avec le partenaire le plus électrophile, qui dans ce cas est le carbone du groupe carbonyle de l'aldéhyde lui-même.
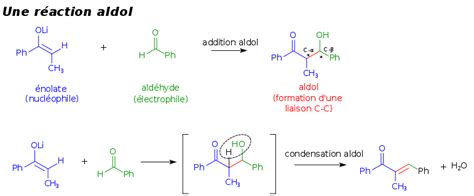
La mention de "quatre produits" dans le contexte de l'examen suggère une simplification ou une focalisation sur les voies réactionnelles les plus probables ou les plus étudiées dans ce cas précis. Il est possible que les quatre produits considérés soient ceux résultant de l'attaque des énolates les plus réactifs de la dicétone sur l'aldéhyde, et potentiellement l'auto-condensation de l'aldéhyde, si celui-ci est le partenaire électrophile. La dicétone, étant plus fonctionnalisée, présente une réactivité accrue. L'énolate cinétique de la dicétone sera formé par déprotonation du méthyle terminal (C1 ou C5), tandis que l'énolate thermodynamique proviendra de la déprotonation du méthylène central (C3).
Un autre exemple classique de ce phénomène se trouve dans l'addition électrophile sur des diènes conjugués, comme le buta-1,3-diène. La réaction avec le bromure d'hydrogène (HBr) peut conduire à deux produits principaux :
Addition 1,2 : Formation du 3-bromo-1-butène. Ce produit est issu de l'addition du H+ sur le C1 et du Br- sur le C2. Il s'agit du produit cinétique, formé le plus rapidement en raison d'une barrière d'activation plus faible. L'état de transition menant à ce produit est souvent moins encombré.
Addition 1,4 : Formation du 1-bromo-2-butène. Ce produit résulte de l'addition du H+ sur le C1 et du Br- sur le C4. Il s'agit du produit thermodynamique, plus stable. La stabilité accrue provient de la formation d'une double liaison interne plus substituée et de la stabilisation par résonance du cation allylique intermédiaire.
L'explication de ces sélectivités inversées repose sur la nature du cation allylique intermédiaire, stabilisé par mésomérie. L'addition du nucléophile (Br-) sur ce cation peut se faire en position 2 (addition 1,2) ou en position 4 (addition 1,4).
Contrôle Cinétique (Basses Températures) : À basses températures, la réaction est arrêtée avant que l'équilibration ne puisse se produire. Le produit cinétique (addition 1,2) est favorisé car il se forme plus rapidement. Le cation allylique intermédiaire est protoné en C1, créant un carbocation en C2. L'attaque du bromure sur le C2 est rapide.
Contrôle Thermodynamique (Hautes Températures) : À températures élevées, le système a le temps d'atteindre l'équilibre. L'intermédiaire cationique allylique peut se réarranger, et l'addition du bromure se fait préférentiellement en position 4, conduisant au produit le plus stable (addition 1,4). Les températures élevées permettent la réversibilité des étapes, favorisant la formation du produit le plus stable. Il est même possible, après l'atteinte de l'équilibre à haute température, de refroidir lentement pour déplacer davantage l'équilibre vers le produit thermodynamique.
La confusion concernant le "ALL" dans les solutions pour la question 3(a)(ii) semble liée à une interprétation potentielle de l'étendue des réactifs possibles. Si l'énoncé stipule quatre produits, cela signifie que le système réactionnel, sous les conditions spécifiées, conduit effectivement à quatre composés distincts.
Si, dans votre cours, l'exemple de la 2,4-hexanedione en tant qu'énolate suggère davantage de possibilités, il est probable que ces possibilités soient soit :
Il est donc crucial de se référer aux conditions exactes de la question pour comprendre pourquoi seulement quatre produits sont attendus. La mention "ALL" pourrait signifier que toutes les combinaisons des réactifs spécifiés qui mènent à des produits distincts sont à considérer, et non pas une infinité de possibilités théoriques.
Pour consolider votre compréhension et pratiquer ces concepts, voici quelques pistes :
En résumé, la distinction entre le contrôle cinétique et thermodynamique est fondamentale en chimie organique. Le contrôle thermodynamique exige des conditions d'équilibration, permettant au produit le plus stable de se former, tandis que le contrôle cinétique favorise le produit formé le plus rapidement. Comprendre ces principes et les facteurs qui les influencent (base, température, temps de réaction) est essentiel pour maîtriser la sélectivité des réactions impliquant des énolates et d'autres intermédiaires réactionnels.
tags: #enolate #cinetique #et #thermodynamique