La purification des peptides et des protéines est une étape fondamentale et souvent complexe dans le domaine de la protéomique et de la recherche biomédicale. Que ce soit pour des études structurelles, des dosages biochimiques in vitro, ou comme préparation essentielle avant des analyses de pointe telles que la LC-MS, l'obtention de composés purs est primordiale. Diverses techniques chromatographiques, incluant l'affinité, l'échange d'ions, l'exclusion de taille, la chromatographie en phase inverse, et la filtration sur gel, sont couramment employées. Cependant, des méthodes plus rapides et efficaces, telles que l'extraction en phase solide (SPE) et l'utilisation de billes magnétiques, gagnent en popularité pour leur polyvalence et leur rapidité. Cet article explore en détail les différentes étapes et considérations relatives à la purification de peptides, en mettant l'accent sur l'utilisation des technologies ZipTip et des systèmes HPLC, tout en considérant les nuances influençant l'efficacité de ces processus.
Les peptides, constitués d'acides aminés liés par des liaisons peptidiques, présentent des propriétés physico-chimiques variées qui dictent leur comportement lors des processus de purification. Ils sont amphiprotiques, possédant à la fois des groupes fonctionnels faiblement acides (acide carboxylique) et faiblement basiques (amine), ce qui leur confère un caractère zwitterionique. Le point isoélectrique (pI), défini comme la concentration d'ions hydrogène à laquelle un peptide ne migre pas sous l'effet d'un champ électrique, est une propriété clé qui influe sur leur comportement chromatographique.
L'objectif principal de tout système de purification est de conserver la plus grande quantité de protéines ou de peptides fonctionnels tout en éliminant un maximum de contaminants. Ceci doit être accompli dans le plus petit nombre d'étapes possible pour minimiser les risques de dénaturation, d'agrégation, de dégradation ou de perte de fonction. La planification minutieuse de la méthode de purification, en tenant compte de l'application en aval de la protéine ou du peptide purifié, est donc essentielle. La quantité et la pureté requises pour l'analyse expérimentale, ainsi que la nécessité de maintenir la conformation native et fonctionnelle, doivent guider le choix des techniques et des conditions opératoires.
Avant des analyses sensibles comme la LC-MS, le dessalage des peptides est une étape de préparation d'échantillons protéomiques cruciale. Ce processus vise à éliminer les sels et autres contaminants qui pourraient interférer avec l'analyse, garantissant ainsi une meilleure sensibilité et une qualité de données accrue. L'extraction en phase solide (SPE) est l'une des méthodes les plus couramment utilisées pour cette tâche.
Les systèmes ASPEC® incarnent une approche polyvalente, combinant l'extraction en phase solide à pression positive, une manipulation précise des liquides, une grande capacité de plateau et une intégration directe aux systèmes de chromatographie liquide. Parmi les technologies SPE, les pointes de pipettes ZipTip offrent une solution pratique et efficace pour la préparation d'échantillons à petite échelle.
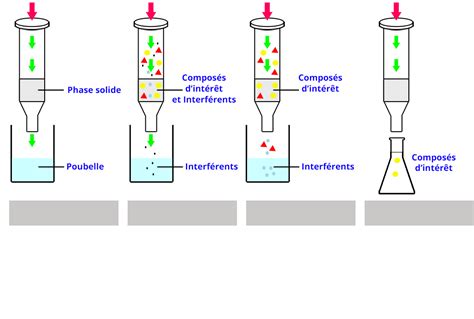
Les ZipTips sont disponibles avec différentes résines, notamment C18, C4 et SCX, chacune offrant des propriétés d'interaction distinctes.
ZipTip C18 et µ-C18 : Ces pointes utilisent une silice sphérique C18 de 15 µm avec une taille de pore de 200 Å. Elles sont idéales pour le dessalage d'oligonucléotides et de peptides ou protéines de faible poids moléculaire (jusqu'à 50 000 Da). Le ZipTip C18 standard a un volume de lit de 0,6 µL permettant une élution en 1 à 4 µL, tandis que le ZipTip µ-C18, avec un micro-lit de 0,2 µL, permet une élution en moins de 1 µL. La capacité de liaison typique pour le C18 est supérieure ou égale à 1 µg, souvent autour de 5,0 µg.
ZipTip C4 : Cette résine est particulièrement adaptée au dessalage de protéines de faible à intermédiaire poids moléculaire (3 000 - 100 000 Da), avec une élution finale en 1 à 4 µL. Sa capacité de liaison typique est d'environ 3,3 µg. L'utilisation d'un agent chaotropique, tel que le Guanidine HCl (1-4M), peut être nécessaire pour améliorer l'adsorption lorsque la solubilité du peptide ou de la protéine est un problème.
Les volumes d'élution pour les ZipTips à lit standard sont généralement de 1 à 4 µL, tandis que les ZipTips µ-C18 ont un volume d'élution inférieur à 1 µL. Ces pointes sont compatibles avec la plupart des pipettes monocanaux acceptant les embouts de 10 ml. Pour le traitement de plusieurs échantillons, la pipette multicanaux Biohit Proline® est recommandée pour un traitement à 8 canaux.
La préparation d'échantillons avant l'analyse MALDI-TOF MS ou l'injection directe en ESI/nanoESI MS est une application courante des ZipTips. La capacité de liaison typique des ZipTips est de 3,3 µg pour le C4 et le µ-C18, et supérieure ou égale à 1 µg (souvent 5,0 µg) pour le C18 standard. La gamme de température d'utilisation s'étend de 4 à 70 °C, avec une stabilité au pH de 1,5 à 13,5 (et 2 à 12 pour une exposition de 24 heures).
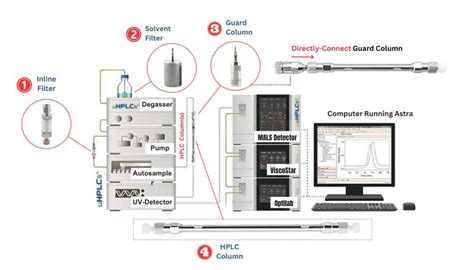
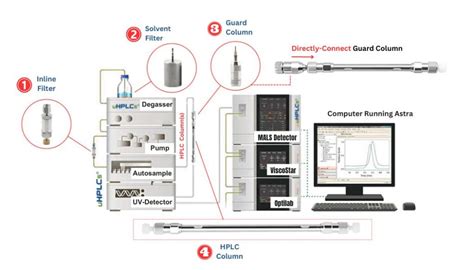
La chromatographie liquide haute performance (HPLC) est une technique puissante pour la séparation et la purification des peptides et des protéines. Les systèmes HPLC, tels que le VERITY® 271 LCMS, offrent une plateforme polyvalente pour des purifications semi-préparatives à préparatives, associées à diverses options de détection.
Ces systèmes permettent l'intégration de capacités d'injection et de collecte de fractions au sein d'une seule plateforme. Les détecteurs disponibles incluent le VERITY® 1741 UV/VIS, le VERITY® 1601 ELS (détecteur évaporatif à diffusion de lumière), ainsi que le suivi de la conductivité et du pH avec le VERITY® 1810. Le détecteur UV-VIS VERITY® 1741, en particulier, est conçu pour les systèmes de purification semi-préparatifs à préparatifs, offrant une détection à balayage multi-longueurs d'onde avec un faible coût de fonctionnement.
Le VERITY® 1920 MS, un spectromètre de masse, est idéal pour les laboratoires recherchant une détection par MS efficace pour isoler des composés purs. Sa polyvalence réside dans sa capacité à utiliser des sources d'ionisation par électronébulisation (ESI) ou par ionisation chimique à pression atmosphérique (APCI), le rendant adaptable à diverses applications.
Le choix de la phase stationnaire, ou colonne, est déterminant pour l'efficacité de la purification des peptides. L'idéal serait d'utiliser une seule chimie de colonne pour tous les types d'échantillons, qu'il s'agisse de peptides ordinaires, basiques, volumineux (30-40 résidus) ou hydrophobes. Cela simplifierait la gestion des stocks et réduirait le temps consacré au développement de méthodes.
Bien que les phases C18 soient couramment utilisées, la nature de la particule de base greffée influence considérablement le temps de rétention, la résolution et la finesse des pics. Les colonnes XBridge Peptide BEH, basées sur des particules hybrides à ponts éthane plutôt que sur de la silice pure, minimisent les interactions secondaires avec les peptides et sont stables sur une large gamme de pH (acide et basique), offrant une flexibilité maximale. Ces particules hybrides (BEH - éthylsiloxane/silice ponté) sont disponibles avec une porosité de 130 Å ou 300 Å et des granulométries de 3,5, 5 et 10 µm.

Des études ont montré que la colonne XBridge Peptide BEH C18 de 130 Å est particulièrement bien adaptée à la purification des peptides. L'évaluation sur un panel de quatre peptides aux propriétés différentes a confirmé cette observation.
La porosité de la colonne peut également jouer un rôle dans la séparation des peptides volumineux ou hydrophobes. Pour un peptide de 39 résidus et une masse moléculaire supérieure à 4 000 Da, une légère amélioration de la finesse des pics a été observée avec une phase stationnaire à pores plus larges (300 Å), le peptide éluant légèrement plus tôt. De même, un peptide hydrophobe avec un indice HPLC élevé élue sous forme de pic symétrique et net avec des phases stationnaires de 130 Å et 300 Å. La conformation du peptide en solution peut également influencer le choix de la porosité.
La granulométrie de la phase stationnaire est un facteur important pour la purification à plus grande échelle, influençant les coûts et l'efficacité. Bien que des granulométries plus importantes puissent entraîner des pics plus larges et une résolution moindre, la sélectivité chimique des colonnes BEH reste constante. Une granulométrie plus élevée est avantageuse pour les purifications à grande échelle, permettant des débits plus rapides sur des colonnes de plus grand diamètre tout en gérant la pression.
La phase mobile, composée d'un solvant faible, d'un solvant fort et d'un modificateur, est essentielle pour la séparation chromatographique. En chromatographie en phase inverse, le solvant faible est généralement de l'eau, tandis que l'acétonitrile est souvent préféré comme solvant fort en raison de sa faible viscosité, de sa force légèrement supérieure et de sa compatibilité avec la détection UV. L'acétonitrile offre généralement la meilleure finesse de pic, s'évapore facilement et réduit les réactions secondaires.
Cependant, pour des raisons de biocompatibilité ou pour améliorer la solubilité de peptides volumineux ou hydrophobes, des alcools comme l'éthanol ou l'isopropanol peuvent être utilisés en remplacement ou en mélange avec l'acétonitrile. Un mélange isopropanol/acétonitrile à 70:30 peut améliorer la résolution du pic principal et réduire le temps de rétention.
La purification des peptides par chromatographie en phase inverse nécessite l'ajout d'un modificateur polaire à la phase mobile pour surmonter les charges positives et négatives des peptides, qui réduisent leur affinité pour la surface hydrophobe de la phase stationnaire. Les modificateurs contrôlent le pH, modifiant ainsi le degré d'ionisation des chaînes latérales.
Acide Formique (FA) : Abaisse le pH, protonant les chaînes latérales acides et réduisant la charge négative, ce qui augmente l'attraction vers la surface hydrophobe. Bien que la plupart des silanols soient protonés, des silanols libres peuvent encore se lier au peptide.
Acide Trifluoroacétique (TFA) : Le modificateur le plus couramment utilisé. Son mécanisme d'interaction implique la protonation des chaînes latérales acides et l'appariement d'ions pour neutraliser les chaînes latérales basiques, inhibant leur liaison aux silanols libres et réduisant la traînée des pics. Les colonnes à particules hybrides à ponts éthane éliminent les interactions avec les silanols, rendant l'utilisation du TFA moins critique pour la réduction de la traînée. Le FA ou le TFA peuvent être utilisés pour modifier la sélectivité tout en conservant une bonne finesse de pics.
pH basique (Bicarbonate d'ammonium, Hydroxyde d'ammonium) : L'élévation du pH déprotone et ionise les chaînes latérales acides, tout en déprotonant et neutralisant les chaînes latérales basiques, réduisant la charge du peptide et augmentant son attraction pour la surface hydrophobe. Le bicarbonate d'ammonium est volatil et facile à éliminer.
L'utilisation de pH extrêmes modifie la sélectivité. Un peptide acide présente une rétention plus longue à pH acide, tandis qu'à pH basique, sa rétention est plus courte en raison d'un plus grand nombre de charges négatives. Un peptide basique montre un comportement inverse : à pH basique, ses résidus basiques sont déprotonés, entraînant une forte interaction avec la colonne nécessitant une proportion plus élevée de solvant organique pour l'élution.
Il est crucial de rappeler que les conditions de pH extrêmes ne doivent pas être utilisées avec des colonnes à base de silice, car un pH trop acide peut cliver la phase greffée et un pH basique peut détruire le support de colonne.
Le contrôle de la température est un paramètre important pour la reproductibilité des séparations et peut offrir des avantages significatifs pour la purification, notamment pour les peptides hydrophobes à faible solubilité. L'augmentation de la température améliore la solubilité et la finesse des pics. Bien que moins couramment utilisé en chromatographie préparative qu'en analytique, le chauffage de la colonne peut optimiser les séparations.
Pour un chauffage efficace des colonnes de grand diamètre, il est recommandé de placer une boucle de préchauffage du solvant à la tête de la colonne et d'immerger la boucle et la colonne dans un bain-marie. La boucle de préchauffage, constituée d'une tubulure de diamètre interne étroit, a un impact négligeable sur l'élargissement des pics.
Des études ont démontré l'effet du contrôle de température sur la séparation de peptides. Par exemple, un peptide basique a montré une meilleure séparation à 60 °C, tandis qu'un peptide acide était mieux séparé à 40 °C.
La purification des protéines, tout comme celle des peptides, repose sur l'isolement basé sur des différences de propriétés physiques. Les techniques courantes incluent la chromatographie d'affinité (notamment avec des tags HIS, GST, FLAG), la chromatographie échangeuse d'ions, la chromatographie d'interaction hydrophobe et la chromatographie d'exclusion de taille. L'utilisation de plusieurs de ces méthodes en séquence est souvent nécessaire pour atteindre la pureté requise.
Les additifs couramment utilisés dans les tampons de purification, tels que les inhibiteurs de protéase, les chélateurs de métaux (EDTA, EGTA), les osmolytes (glycérol), les détergents et les sels, jouent un rôle dans le maintien de la stabilité et de la fonction des protéines. Ces additifs ne doivent être utilisés que lorsque cela est nécessaire.
Le principe de la chromatographie sur colonne consiste à séparer un mélange de protéines en fractions enrichies en protéine d'intérêt. L'équipement de base comprend la phase stationnaire (matrice), la colonne, les solvants et les tubes de prélèvement. Les systèmes automatisés, comme ceux proposés par GE Healthcare (FPLC AKTA), offrent une grande reproductibilité et la possibilité de programmer des gradients d'élution, mais nécessitent un investissement matériel plus important. Les systèmes par gravité sont moins coûteux mais demandent plus de travail manuel.
La chromatographie d'affinité, exploitant une interaction spécifique entre une protéine et un ligand, est souvent utilisée dans les premières étapes de purification en raison de sa robustesse. Les autres techniques chromatographiques se basent sur des propriétés différentes : la charge nette pour l'échange d'ions, l'hydrophobicité pour l'interaction hydrophobe, et le rayon hydrodynamique pour l'exclusion de taille.
Le développement de méthodes de séparation peut nécessiter l'ajustement de divers paramètres tels que le solvant de la phase mobile, le modificateur, la pente du gradient, la température, le pH ou la méthode d'introduction de l'échantillon. L'utilisation d'une colonne unique avec une technologie de particules hybrides stables, comme la technologie XBridge Peptide BEH, peut simplifier le processus de purification en réduisant le nombre de colonnes nécessaires.
En résumé, la purification des peptides et des protéines est un processus multi-facettes qui bénéficie de l'intégration de technologies avancées telles que les ZipTips pour la préparation d'échantillons et les systèmes HPLC pour la séparation. Une compréhension approfondie des propriétés des peptides, combinée à une optimisation rigoureuse des paramètres chromatographiques (choix de la colonne, composition de la phase mobile, pH, température), est essentielle pour obtenir des résultats de haute qualité.
tags: #differentes #etapes #de #la #purification #ziptip