La synthèse de l'aspirine, également connue sous le nom d'acide acétylsalicylique, est une expérience fondamentale en chimie organique qui permet d'illustrer des concepts clés tels que les réactions de substitution, l'utilisation de groupes protecteurs et, de manière cruciale, les techniques de purification. Parmi ces dernières, la recristallisation occupe une place de choix pour isoler des composés solides sous forme cristalline pure. Cette méthode exploite les différences de solubilité entre le produit désiré et les impuretés dans un solvant donné, à différentes températures.
La synthèse de l'aspirine implique typiquement la réaction entre l'acide salicylique et l'anhydride acétique. L'acide salicylique (C7H6O3) possède une fonction acide carboxylique et une fonction alcool. L'anhydride acétique, ou anhydride éthanoïque, agit comme agent d'acétylation, introduisant un groupe acétyle sur la fonction alcool de l'acide salicylique. Cette réaction est une réaction de substitution, où le groupe hydroxyle de l'acide salicylique est substitué par un groupe acétyle.
Pour accélérer cette réaction et minimiser les pertes de réactifs et de produits, un montage à reflux est souvent utilisé. Ce montage permet de chauffer le mélange réactionnel à son point d'ébullition sans perte de matière volatile, car les vapeurs sont condensées et retournent dans le ballon. L'anhydride éthanoïque est un réactif très irritant pour les yeux, et des précautions doivent être prises lors de sa manipulation. Il est important de noter que dans ce type de synthèse, l'anhydride acétique est généralement utilisé en excès, tandis que l'acide salicylique est le réactif limitant. La réaction se fait de manière quasi stœchiométrique (mole à mole). Le nom "éthanoïque" fait référence à la présence de deux groupes acétyles dans l'anhydride acétique.
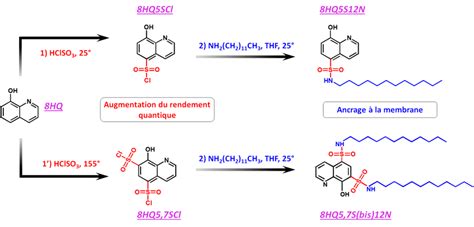
Après la réaction, l'addition d'eau au mélange refroidi permet d'hydrolyser l'excès d'anhydride acétique restant, le transformant en acide acétique, qui est très miscible à l'eau. Cette étape conduit à la formation d'un solide brut, désigné ici comme S1, qui correspond à l'aspirine impur précipité.
La recristallisation est une technique de purification essentielle pour les composés solides obtenus lors de transformations chimiques. Elle repose sur le principe fondamental que la solubilité d'un solide dans un solvant donné varie généralement avec la température. Le processus vise à dissoudre le solide impur dans un minimum de solvant chaud, puis à laisser la solution refroidir lentement. Au fur et à mesure que la température diminue, la solubilité du composé désiré diminue, entraînant sa cristallisation. Les impuretés, idéalement, restent solubles dans le solvant froid ou ont des propriétés de solubilité suffisamment différentes pour ne pas co-précipiter avec le produit principal.
Choix du Solvant : Une Étape Cruciale
Le choix du solvant de recristallisation est primordial pour le succès de la purification. Le solvant idéal doit présenter les caractéristiques suivantes :
Dans le cas de la purification de l'aspirine, l'eau, un mélange eau-éthanol, ou l'éthanol lui-même peuvent être utilisés comme solvants, en fonction de la nature des impuretés.
Mise en Œuvre de la Recristallisation
Le solide brut S1 est placé dans un ballon et dissous dans un minimum de solvant chaud. Il est souvent nécessaire de chauffer la solution jusqu'à ce qu'elle soit limpide, signe que tout le produit désiré est dissous. Si des impuretés insolubles sont présentes à chaud, une filtration à chaud peut être effectuée à l'aide d'un entonnoir à solide, éventuellement avec un filtre et une étuve, pour les éliminer avant le refroidissement.
Une fois la solution limpide et exempte d'impuretés insolubles, elle est laissée refroidir. Un refroidissement lent est généralement préférable pour permettre la formation de cristaux bien formés et éviter d'emprisonner des impuretés à l'intérieur du réseau cristallin. Le refroidissement peut être initié à température ambiante, puis accéléré en plaçant le récipient dans un bain d'eau glacée, comme indiqué par la formation de cristaux S2.
Le lavage des cristaux S2 avec de l'eau glacée est une étape cruciale pour minimiser les pertes de produit. L'eau glacée abaisse la température de la suspension de cristaux, réduisant ainsi la solubilité de l'aspirine dans le solvant. En lavant les cristaux avec de l'eau glacée, on élimine la liqueur mère (la solution restante contenant les impuretés solubles) qui adhère à la surface des cristaux, sans pour autant dissoudre une quantité significative d'aspirine purifiée. Si l'on utilisait de l'eau à température ambiante ou chaude, une partie du produit désiré se dissoudrait et serait perdue lors de la filtration.
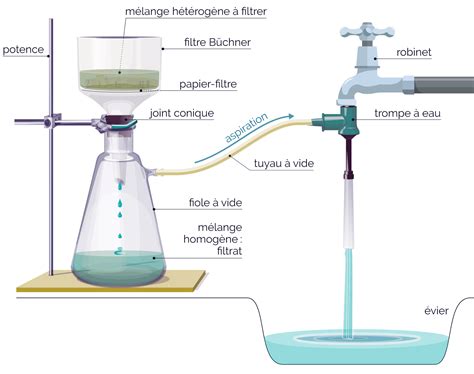
Une fois la cristallisation terminée, les cristaux S2 sont récupérés par filtration. La filtration sous vide, utilisant une trompe à eau et un filtre Büchner, est une méthode efficace pour séparer rapidement les cristaux du solvant. Le solide est ensuite lavé une dernière fois avec une petite quantité de solvant froid pour éliminer toute trace de liqueur mère résiduelle.
Le solide obtenu est ensuite séché pour éliminer toute trace de solvant. Le séchage peut se faire à l'air libre, dans une étuve à basse température, ou sous vide.
La pureté des cristaux obtenus peut être évaluée par différentes méthodes :
Ces méthodes permettent de confirmer le succès de la purification par recristallisation.
Les changements d'état sont fondamentaux dans les processus de séparation et de purification en chimie. La recristallisation exploite directement la différence de solubilité, qui est une propriété liée aux changements d'état et aux interactions intermoléculaires.
Les impuretés présentes dans le produit brut peuvent provenir de diverses sources : réactifs n'ayant pas réagi, produits secondaires de la réaction, ou contaminants du milieu réactionnel. Leur nature et leur solubilité détermineront l'efficacité de la recristallisation. Par exemple, si une impureté est très soluble à froid comme à chaud, elle restera dans la liqueur mère. Si elle est insoluble à chaud, elle sera éliminée par filtration à chaud.
La formation de cristaux S2 après un lent refroidissement indique que le processus de cristallisation a réussi. L'agitation pendant la formation du précipité S1 peut aider à obtenir des particules plus fines et plus homogènes, facilitant la dissolution ultérieure. Le rinçage du solide avec un peu d'eau après la formation initiale vise à éliminer les réactifs solubles résiduels avant l'étape de recristallisation proprement dite.
La capacité d'une substance à se dissoudre dans un solvant dépend de la nature des forces intermoléculaires entre les molécules du soluté et celles du solvant. Pour l'aspirine, qui est une molécule polaire avec des groupes fonctionnels capables de former des liaisons hydrogène, le choix d'un solvant polaire est souvent approprié. L'acide acétique, sous-produit de l'hydrolyse de l'anhydride acétique, est très soluble dans l'eau, ce qui est avantageux pour son élimination lors de la recristallisation.
L'utilisation d'un bain-marie pour chauffer l'eau à 60°C permet un contrôle précis de la température, essentiel pour une dissolution efficace sans dégrader l'aspirine, qui peut s'hydrolyser en acide salicylique et acide acétique dans des conditions trop chaudes ou prolongées. Le refroidissement dans un cristallisoir contenant de l'eau glacée accélère la cristallisation, maximisant le rendement du produit purifié S2. Il est crucial de ne jamais présenter le visage à l'ouverture du ballon lors du chauffage, en raison des risques de projections de produits chimiques chauds ou irritants.
tags: #synthese #aspirine #purification #par #recristallisation