La purification des protéines est une étape fondamentale et indispensable dans de nombreux domaines de la recherche scientifique, du diagnostic médical à la production de biomédicaments. Elle vise à isoler une ou plusieurs protéines d'intérêt à partir de mélanges biologiques complexes, qu'il s'agisse de tissus, de cultures cellulaires ou de produits de fermentation. Ce processus, bien que souvent complexe, est crucial pour la caractérisation fonctionnelle, structurale et interactionnelle des protéines, ouvrant la voie à une meilleure compréhension des processus biologiques et au développement de nouvelles thérapies.
Avant toute purification, il est nécessaire d'extraire les protéines de leur matrice d'origine. L'extraction de la protéine cible comprend plusieurs étapes clés. Tout d'abord, le broyage des cellules contenant la protéine cible est effectué. Cette rupture cellulaire peut être réalisée par diverses méthodes, adaptées à la nature de la cellule. Pour les tissus végétaux et animaux résistants, l'homogénéisation est souvent privilégiée. Les bactéries, dont la paroi cellulaire est plus robuste, peuvent être traitées par ultrasons. Quant aux levures, le cyclage de pression est une technique efficace.
La destruction des cellules peut également être obtenue par des cycles répétés de congélation-décongélation, par traitement ultrasonique, ou par l'utilisation de détergents. Ces méthodes visent à fragiliser les membranes cellulaires et à libérer le contenu intracellulaire. Une fois les cellules lysées, il est essentiel d'éliminer les débris cellulaires. La centrifugation différentielle est une technique couramment employée à cette fin, permettant de séparer les composants cellulaires en fonction de leur densité et de leur taille. Cette étape est cruciale pour permettre la sécrétion de la protéine dans le milieu environnant ou pour préparer l'échantillon pour les étapes de purification ultérieures.
Les méthodes spécifiques d'extraction de protéines sont variées :
L'ajout d'une quantité appropriée de tampon ou d'inhibiteur de protéase est une précaution indispensable pour prévenir la dégradation des protéines par les enzymes endogènes. Il est également nécessaire d'assurer la solubilité des protéines dans la solution et d'empêcher leur agrégation, deux phénomènes qui peuvent compromettre la réussite de la purification.
La production de protéines recombinantes est une biotechnologie puissante qui permet d'obtenir des protéines d'intérêt en grande quantité. Ce processus implique l'introduction d'ADN recombinant, porteur du gène codant pour la protéine souhaitée, dans des cellules hôtes capables d'exprimer ce gène. Divers systèmes d'expression sont couramment utilisés, incluant les bactéries (comme Escherichia coli ou Bacillus subtilis), les levures (Saccharomyces cerevisiae, Pichia pastoris), les cellules d'insectes, ou encore les cellules de mammifères.
Le protocole d'expression de protéines recombinantes se déroule généralement en plusieurs étapes :
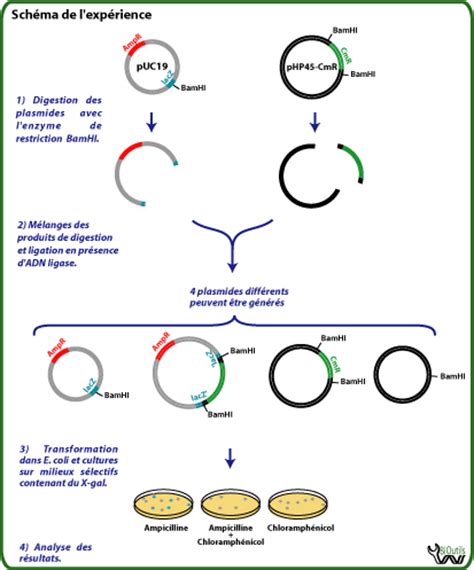
L'objectif principal de la purification des protéines est d'isoler la protéine d'intérêt avec la plus grande pureté possible, tout en préservant son activité biologique et sa structure native. Pour ce faire, une variété de techniques chromatographiques et non chromatographiques sont employées, exploitant les différences de propriétés physico-chimiques entre la protéine cible et les contaminants.
La chromatographie est une méthode de séparation puissante qui repose sur la distribution différentielle d'un mélange entre une phase stationnaire et une phase mobile. Plusieurs types de chromatographie sur colonne sont couramment utilisés dans la purification des protéines, chacun exploitant un principe de séparation distinct :
Chromatographie d'Affinité : Cette technique est souvent la plus efficace et est généralement utilisée en première étape. Elle repose sur l'interaction spécifique et réversible entre la protéine d'intérêt et un ligand immobilisé sur une matrice. Ce ligand peut être un anticorps, un substrat enzymatique, un cofacteur, ou même une étiquette (tag) ajoutée à la protéine recombinante. L'affinité de la protéine pour le ligand permet de la capturer sélectivement, tandis que les contaminants ne se lient pas et sont éliminés par lavage. L'élution de la protéine se fait ensuite en utilisant un compétiteur du ligand ou en modifiant les conditions (pH, force ionique) pour rompre l'interaction.
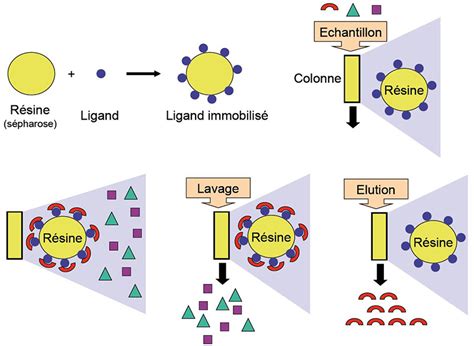
Les protéines recombinantes sont souvent produites avec des "étiquettes" (tags) qui facilitent grandement leur purification par chromatographie d'affinité. Parmi les étiquettes les plus courantes, on trouve :
Chromatographie d'Échange d'Ions (IEX) : Cette méthode sépare les protéines en fonction de leur charge nette, qui varie avec le pH du tampon. Les résines d'échange d'ions portent des groupes chargés positivement (échangeurs d'anions) ou négativement (échangeurs de cations). Les protéines portant une charge opposée à celle de la résine se lient, tandis que celles de même charge ou neutres sont éluées. L'élution des protéines liées se fait en augmentant progressivement la force ionique du tampon (avec des sels comme NaCl) ou en modifiant le pH pour neutraliser la charge de la protéine. Le choix de la résine (cationique ou anionique) et du pH dépend du point isoélectrique (pI) de la protéine d'intérêt.
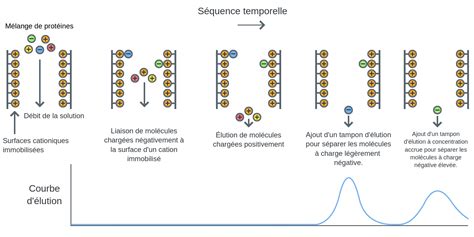
Chromatographie d'Interaction Hydrophobe (HIC) : Cette technique sépare les protéines en fonction de leur hydrophobicité. En présence d'une forte concentration de sels (comme le sulfate d'ammonium), les régions hydrophobes des protéines, normalement enfouies à l'intérieur de la structure, sont exposées et interagissent avec des groupes hydrophobes immobilisés sur la phase stationnaire. L'élution s'obtient en diminuant progressivement la force ionique du tampon, ce qui permet aux protéines de retrouver leur enveloppe d'hydratation et de se détacher de la résine. La HIC est particulièrement utile pour les protéines qui peuvent se replier spontanément.
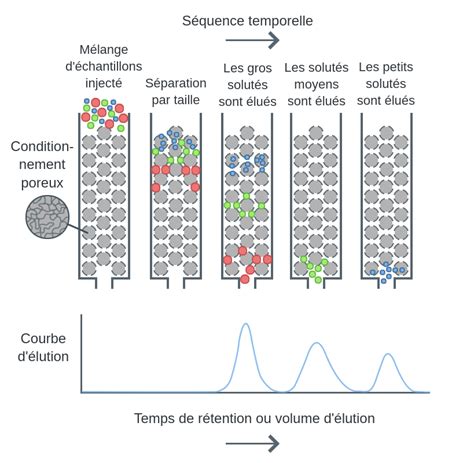
Chromatographie d'Exclusion Stérique (SEC) ou Chromatographie de Filtration sur Gel : Aussi connue sous le nom de chromatographie par perméation de gel, cette méthode sépare les molécules en fonction de leur taille et de leur forme hydrodynamique. La phase stationnaire est constituée de billes poreuses. Les grosses molécules, trop volumineuses pour pénétrer dans les pores, passent rapidement à travers la colonne et sont éluées en premier. Les petites molécules, quant à elles, pénètrent dans les pores, ce qui augmente leur cheminement à travers la colonne et retarde leur élution. Les protéines sont ainsi éluées par ordre décroissant de taille. La SEC est souvent utilisée comme étape finale de polissage pour éliminer les agrégats ou les fragments de protéines.
Chromatographie Liquide à Haute Performance (HPLC) : Bien qu'elle ne soit pas un type de séparation en soi, l'HPLC est une technique qui utilise des pressions élevées pour faire passer la phase mobile à travers une colonne remplie de particules très fines, offrant ainsi une résolution et une efficacité de séparation exceptionnelles. L'HPLC peut être couplée à divers modes de séparation (affinité, échange d'ions, etc.) pour des purifications de haute précision. Elle est particulièrement utile pour la purification de peptides et de petites protéines.
Outre la chromatographie, d'autres méthodes sont employées pour la purification ou la préparation des échantillons protéiques :
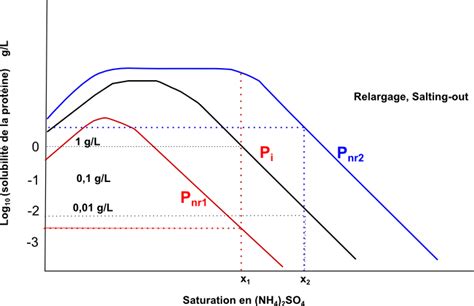
Précipitation : Cette technique exploite la différence de solubilité des protéines. La précipitation par le sulfate d'ammonium, par exemple, permet d'isoler des fractions protéiques en ajoutant progressivement le sel, qui réduit la solubilité des protéines en interagissant avec l'eau. Les protéines précipitées sont ensuite récupérées par centrifugation.
Ultrafiltration et Dialyse : Ces techniques sont utilisées pour la concentration des solutions protéiques et le dessalement (élimination des sels). L'ultrafiltration utilise une membrane semi-perméable pour retenir les macromolécules (protéines) tout en laissant passer l'eau et les petites molécules. La dialyse permet l'échange de solutés entre la solution protéique et un tampon externe à travers une membrane semi-perméable, facilitant ainsi l'élimination des impuretés de faible masse moléculaire.
Le maintien de la stabilité et de la fonction des protéines pendant leur purification est primordial. Les conditions de la solution, notamment le pH, jouent un rôle essentiel. Les tampons sont des solutions contenant une paire d'acide/base conjugués qui résistent aux changements brusques de pH.
Un bon tampon doit présenter plusieurs caractéristiques : solubilité dans l'eau, stabilité chimique, grande capacité tampon au pH désiré, compatibilité avec les applications analytiques et expérimentales, et compatibilité avec les autres composants de la solution. Parmi les tampons biologiques couramment utilisés, on trouve le phosphate, le MOPS, le HEPES et le Tris. Le choix du tampon et sa concentration (souvent supérieure à 25 mM) dépendent du pH optimal pour la protéine d'intérêt et de la compatibilité avec les étapes chromatographiques ultérieures.
En plus d'un système tampon approprié, divers additifs peuvent être ajoutés aux solutions de purification pour améliorer la stabilité et la fonction des protéines :
Il est important de noter que les additifs ne doivent être utilisés que si nécessaire, et que la minimisation des étapes de manipulation et la rapidité du processus sont des facteurs clés pour obtenir un rendement élevé de protéines fonctionnelles. Le maintien de la protéine à basse température tout au long de la purification est également une pratique courante.
Une fois la protéine purifiée, il est essentiel de l'analyser et de la caractériser pour confirmer sa pureté, sa concentration, son activité et sa structure.
Plusieurs méthodes colorimétriques sont utilisées pour quantifier la concentration des protéines :
La pureté d'un échantillon protéique est généralement évaluée par des techniques électrophorétiques et de transfert :
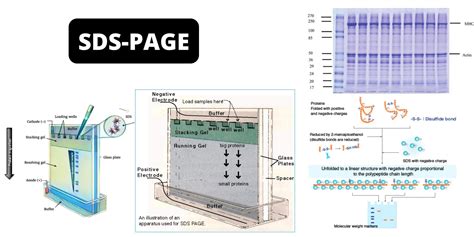
SDS-PAGE (Électrophorèse sur Gel de Polyacrylamide en Présence de Dodécylsulfate de Sodium) : Cette technique sépare les protéines principalement en fonction de leur masse moléculaire. Les protéines sont dénaturées par le SDS, qui leur confère une charge négative uniforme. Elles migrent ensuite dans un gel de polyacrylamide sous l'effet d'un champ électrique, les plus petites protéines migrant plus rapidement. La masse moléculaire mesurable se situe généralement entre 5 et 250 kDa. La présence de bandes multiples indique la présence d'impuretés.
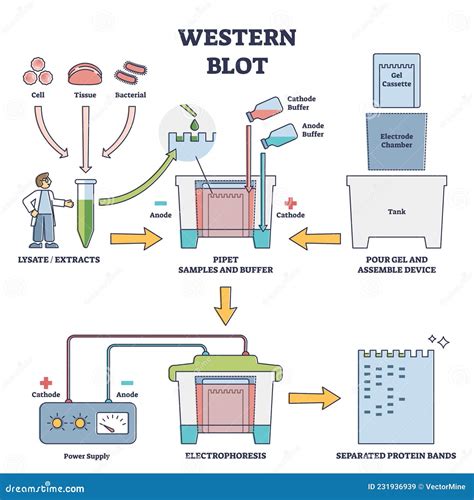
Western Blot : Cette technique combine la SDS-PAGE avec une étape de transfert et de détection immunologique. Après séparation par SDS-PAGE, les protéines sont transférées sur une membrane (PVDF ou nitrocellulose). La protéine cible est ensuite détectée spécifiquement par un anticorps primaire, suivi d'un anticorps secondaire marqué par une enzyme. L'ajout d'un substrat révélant la couleur permet de visualiser et de quantifier la protéine d'intérêt.
ELISA (Dosage immuno-enzymatique) : L'ELISA est une technique très sensible utilisée pour détecter et quantifier des antigènes ou des anticorps. Dans le contexte de la purification protéique, une forme d'ELISA peut être utilisée pour détecter la présence de la protéine cible dans différentes fractions. L'antigène est fixé sur un support solide, puis un anticorps spécifique est ajouté. Un second anticorps marqué par une enzyme permet de générer un signal coloré après addition d'un substrat.
Pour une compréhension approfondie des protéines, des analyses structurales et des interactions sont réalisées :
La purification des protéines est un processus itératif et souvent exigeant, mais essentiel pour la recherche biologique et le développement biotechnologique. La combinaison judicieuse des différentes techniques d'extraction, de purification et d'analyse permet d'obtenir des protéines de haute qualité, ouvrant la voie à des découvertes scientifiques majeures et au développement de nouvelles applications thérapeutiques et diagnostiques. L'optimisation de chaque étape, en tenant compte des propriétés spécifiques de la protéine d'intérêt et de l'application en aval, est la clé d'un système de purification efficace.
tags: #purification #proteines #recapitulatif