La gestion des eaux usées et la purification des fluides représentent des enjeux majeurs pour la santé publique et la préservation de l'environnement. Face à la complexité croissante des contaminants présents dans les rejets liquides, qu'ils soient d'origine industrielle, agricole ou domestique, des méthodes de traitement innovantes sont nécessaires pour éliminer efficacement les formes libres et oxydées des polluants. Ces substances, souvent récalcitrantes aux procédés conventionnels, posent des défis significatifs en termes de sécurité de l'eau et de protection des écosystèmes aquatiques. La sécheresse, un phénomène aux conséquences économiques dévastatrices, accentue la nécessité de développer des technologies de traitement et de réutilisation de l'eau performantes.
Les pratiques actuelles en matière d'épuration des eaux usées peinent à éliminer certains polluants émergents et persistants. Ces contaminants, souvent présents à l'état de traces, peuvent néanmoins présenter des dangers avérés pour la santé humaine et les écosystèmes aquatiques. Les réglementations environnementales de plus en plus strictes imposent des limites d'émission toujours plus basses, poussant à la recherche de solutions de traitement plus avancées. Le principe de "zéro déchet liquide" devient un objectif essentiel dans le développement de nouveaux procédés, visant à minimiser, voire éliminer, la production d'effluents concentrés ou de résidus de traitement.
Le traitement par membranes pour les eaux usées représente une technologie prometteuse, bien que souvent coûteuse. Des projets de recherche, tels que le projet ACTIWATE financé par l'UE, explorent des options de traitement pour les effluents concentrés issus de systèmes membranaires. Ces recherches visent à identifier des méthodes efficaces pour prélever les contaminants présents dans ces flux, ouvrant la voie à une meilleure valorisation des ressources et à une réduction de l'impact environnemental.
Les procédés d'oxydation avancée (POA) constituent une famille de méthodes particulièrement efficaces pour la destruction des polluants organiques présents dans les eaux. Ces procédés exploitent la puissance oxydante de radicaux libres hautement réactifs, dont le radical hydroxyle (•OH), considéré comme l'un des oxydants les plus puissants connus. Le radical hydroxyle peut oxyder une vaste gamme de composés organiques, allant jusqu'à leur minéralisation complète en dioxyde de carbone (CO2) et en eau (H2O).
L'efficacité des POA réside dans leur capacité à générer ces radicaux libres in situ, directement dans la matrice aqueuse à traiter. Le potentiel d'oxydation du radical hydroxyle est largement supérieur à celui d'oxydants plus conventionnels comme l'ozone (O3) ou le peroxyde d'hydrogène (H2O2). Sa vitesse de réaction est également phénoménale, étant généralement des millions de fois plus rapide.
Les systèmes POA de pointe combinent ou exploitent plusieurs agents oxydants pour maximiser la production de radicaux hydroxyles. La conception et la fabrication de systèmes intégrés, combinant technologies ultraviolettes (UV), ozone et POA, répondent aux besoins spécifiques des clients industriels et municipaux. Ces technologies visent à offrir des solutions performantes pour l'élimination des polluants organiques jusqu'à leur transformation en espèces chimiques inoffensives.
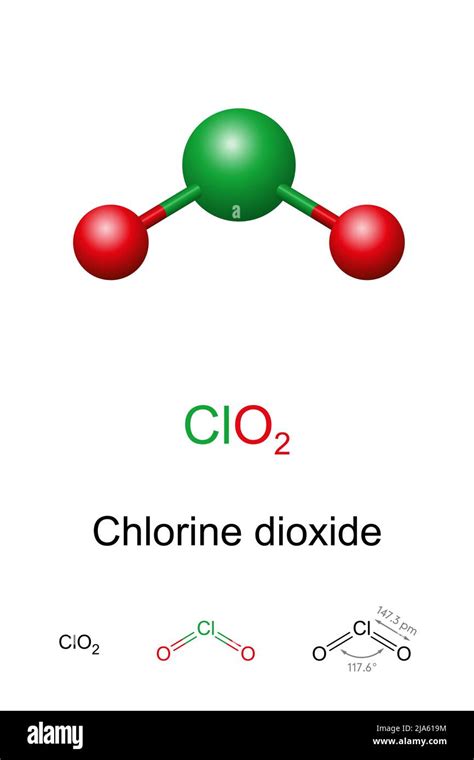
Le dioxyde de chlore (ClO2) est un composé chimique aux propriétés remarquables, trouvant des applications variées en tant qu'agent de blanchiment, désinfectant et oxydant. Découvert en 1814 par Humphry Davy, le ClO2 diffère fondamentalement du chlore élémentaire (Cl2) par sa structure chimique et son comportement. Il s'agit d'un gaz synthétique vert-jaune, volatil et de petite taille, doté d'une odeur irritante.
Le dioxyde de chlore est un radical libre en solution aqueuse diluée. À forte concentration, il réagit vigoureusement avec les agents réducteurs. C'est un gaz instable qui peut se dissocier en chlore, oxygène et chaleur. Sensible à la lumière du soleil, il se désagrège sous l'effet de la photo-oxydation. Les produits de ses réactions incluent le chlorure (Cl-), le chlorite (ClO2-) et le chlorate (ClO3-).
Le ClO2 possède une excellente solubilité dans l'eau, particulièrement dans l'eau froide, et n'entraîne pas d'hydrolyse, restant à l'état de gaz dissout. Il est environ 10 fois plus soluble dans l'eau que le chlore. Bien qu'il puisse être éliminé par aération ou par le dioxyde de carbone, sa stabilité dans l'eau est une qualité essentielle pour son utilisation comme désinfectant.
| Température (°C) | Pression (mm Hg) | Solubilité (g/L) |
|---|---|---|
| 25 | 3.01 | 2.63 |
| 25 | 34.5 | 1.82 |
| 25 | 22.1 | 1.13 |
| 25 | 13.4 | 0.69 |
| 40 | 8.4 | 2.63 |
| 40 | 56.2 | 1.60 |
| 40 | 18.8 | 0.83 |
| 40 | 9.9 | 0.47 |
| 60 | 106.9 | 2.65 |
| 60 | 53.7 | 1.18 |
| 60 | 21.3 | 0.58 |
| 60 | 12.0 | 0.26 |
Tableau 1 : Solubilité du dioxyde de chlore dans l'eau en fonction de la température et de la pression.
En raison de son instabilité et de son potentiel explosif sous pression, le dioxyde de chlore est rarement stocké et est souvent produit sur le site d'utilisation, généralement sous forme de solution aqueuse. La production s'effectue à partir de solutions de chlorite de sodium (NaClO2) ou de chlorate de sodium (NaClO3) en milieu acide. Pour les installations à grande échelle, des procédés plus complexes impliquant du gaz de chlore (Cl2), du chlorite de sodium, du chlorite de sodium hydrogène (NaHClO2) et de l'acide sulfurique sont employés.
Les réactions de production courantes incluent :
Le stockage sous forme liquide à 4°C offre une stabilité relative. Les solutions aqueuses d'environ 1% de ClO2 (10 g/L) peuvent être stockées efficacement si elles sont protégées de la lumière et de la chaleur.
Le dioxyde de chlore trouve de nombreuses applications :
En tant qu'oxydant, le dioxyde de chlore est remarquablement sélectif grâce à son mécanisme d'échange d'un électron. Il attaque les électrons au centre des molécules organiques, se réduisant en ion chlorite (ClO2-). Cette sélectivité le distingue du chlore, qui a tendance à participer à des réactions d'addition et de substitution, modifiant plus radicalement la structure des composés.
Le potentiel d'oxydation du ClO2 est de 0.95 V, inférieur à celui de l'ozone (2.07 V) ou de l'acide hypochloreux (1.49 V). Cependant, sa capacité d'oxydation, mesurée par le nombre d'électrons transférés par mole, est significativement plus élevée. L'atome de chlore dans le ClO2, avec un état d'oxydation de +4, peut accepter jusqu'à 5 électrons lors de sa réduction en chlorure (Cl-), ce qui se traduit par un "chlore disponible" de 263.0%, surpassant largement celui du chlore élémentaire (100%).
| Oxydant | Pouvoir Oxydant | Capacité d'Oxydation |
|---|---|---|
| Ozone (O3) | 2.07 | 2 e- |
| Peroxyde d'hydrogène (H2O2) | 1.78 | 2 e- |
| Acide hypochloreux (HOCl) | 1.49 | 2 e- |
| Acide hypobromeux (HOBr) | 1.33 | 2 e- |
| Dioxyde de chlore (ClO2) | 0.95 | 5 e- |
Tableau 2 : Potentiels d'oxydation de différents oxydants.
Le dioxyde de chlore désinfecte par oxydation. Contrairement au chlore, qui ajoute ou substitue des atomes de chlore, le ClO2 réagit en cédant un électron. Il attaque directement les acides aminés et l'ARN des cellules microbiennes, interrompant des processus cellulaires vitaux comme la production de protéines. Il affecte également la membrane cellulaire en altérant les protéines et les lipides, empêchant ainsi l'absorption et perturbant l'intégrité de la cellule. Pour les virus, il empêche la formation de protéines.
Le ClO2 est particulièrement efficace contre les parasites protozoaires tels que Giardia Lambia et Cryptosporidium, souvent présents dans l'eau et responsables de maladies comme la lambliase et la cryptosporidiose. Une combinaison de l'ozone et du dioxyde de chlore offre une protection optimale contre ces parasites.
Un avantage majeur du ClO2 est que les microorganismes ne peuvent développer de résistance à son action désinfectante, car il agit directement sur les parois cellulaires, indépendamment de la concentration ou du temps de contact. Il est efficace même contre les microorganismes inactifs.
La capacité du dioxyde de chlore à rester gazeux en solution lui confère une excellente capacité de pénétration. Sa molécule, puissante et facilement soluble, peut traverser les couches de bactéries et les biofilms. Il oxyde la matrice de polysaccharide qui maintient le biofilm compact. Les ions chlorites produits lors de cette réaction peuvent ensuite être transformés en dioxyde de chlore dans l'environnement acide formé par la reprise de croissance du biofilm, assurant ainsi une élimination continue.
Le gaz pur de dioxyde de chlore produit moins de sous-produits de désinfection que les oxydants comme le chlore. Contrairement à l'ozone, il ne transforme pas les ions bromure (Br-) en ions bromate (BrO3-) sauf en cas de photolyse. De plus, il ne génère pas de grandes quantités d'aldéhydes, de cétones ou d'autres sous-produits issus de l'ozonation des matières organiques.
La recherche et le développement dans le domaine de la purification des fluides continuent d'innover. Un projet de recherche récent, décrit dans le brevet FR2936509A1, propose un dispositif et un procédé pour l'élimination de composés indésirables dans un fluide, combinant rayonnement UV, photocatalyse et membranes.
Ce dispositif repose sur un réacteur photocatalytique membranaire. Il intègre un système de rayonnement UV, un matériau photocatalytique (comme le TiO2) susceptible d'être irradié, et une membrane séparant deux compartiments. Le fluide à traiter circule dans l'un des compartiments, tandis qu'un fluide contenant de l'oxygène est introduit dans l'autre. La membrane permet le passage des fluides tout en assurant la rétention du photocatalyseur.
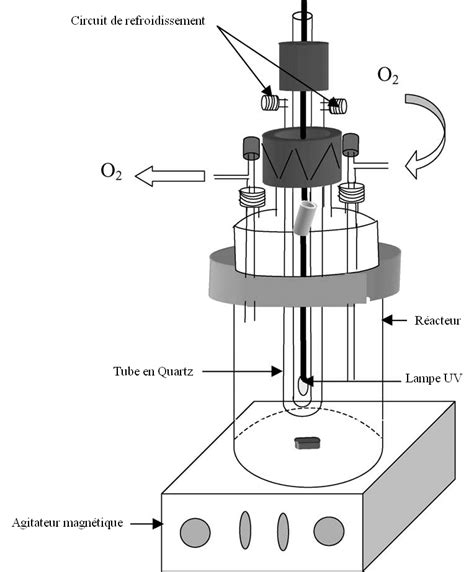
Le principe est d'utiliser l'énergie UV pour activer le matériau photocatalytique, générant des radicaux libres qui vont oxyder les polluants présents dans le fluide. La membrane joue un rôle clé en retenant le photocatalyseur tout en facilitant la diffusion des réactifs et des produits. Cette approche permet d'augmenter la probabilité de rencontre entre les polluants, les radicaux libres et le photocatalyseur activé, améliorant ainsi l'efficacité du traitement.
Les avantages de tels dispositifs résident dans leur compacité, leur efficacité accrue et leur potentiel de réduction des coûts de production. Ils peuvent être adaptés à une large gamme d'applications, de la purification de l'eau potable à la décontamination de l'air, en passant par le traitement des eaux usées industrielles et municipales. L'utilisation de diodes électroluminescentes (LED UV) offre une alternative plus économique et écologique aux lampes à mercure traditionnelles, avec une durée de vie prolongée et une consommation d'énergie réduite.
Ces avancées technologiques ouvrent la voie à des solutions de purification plus durables et plus performantes, essentielles pour relever les défis environnementaux actuels et futurs. La combinaison de différentes technologies, telles que la photocatalyse membranaire et l'utilisation contrôlée d'oxydants puissants comme le dioxyde de chlore, représente une stratégie prometteuse pour l'élimination des formes libres et oxydées des polluants dans les fluides.
tags: #purification #elimination #des #formes #libres #et