L'étude de l'équilibre liquide-vapeur est fondamentale en thermodynamique chimique et trouve des applications dans de nombreux domaines industriels, allant de la pétrochimie à la pharmacie. Comprendre les conditions sous lesquelles les phases liquide et gazeuse d'une substance peuvent coexister est essentiel pour la conception et l'optimisation des processus de séparation, de purification et de stockage. Cet article se propose d'explorer en détail les principes régissant ces équilibres, en se concentrant particulièrement sur le dibrome à 25°C, et en s'appuyant sur des méthodes de calcul et de mesure avancées, ainsi que sur les concepts théoriques sous-jacents.
Avant de plonger dans les spécificités de l'équilibre liquide-vapeur, il est crucial de définir ce que l'on entend par "phase" et "transition de phase". Une phase est une partie d'un système thermodynamique pour laquelle les paramètres intensifs sont uniformes en tout point. Elle est donc intrinsèquement homogène. Un corps pur peut exister sous différentes phases, qui peuvent coexister dans certaines conditions.
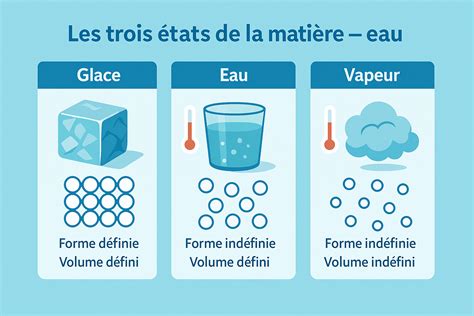
La phase solide se caractérise par une structure microscopique ordonnée et périodique, typique des solides cristallins. La phase liquide, quant à elle, est un état fluide marqué par un désordre moléculaire, mais avec une densité comparable à celle des solides. La phase gazeuse est un fluide peu dense où les molécules sont suffisamment éloignées pour que les interactions moléculaires soient négligeables par rapport à leur énergie cinétique. Un exemple concret de système multi-phasique est un mélange eau/huile, où la discontinuité de densité à l'interface délimite les deux phases. Le carbone illustre également le concept de phases différentes pour un même corps pur, avec le graphite et le diamant comme exemples de phases solides distinctes.
Une transition de phase survient lorsqu'un système passe d'une phase à une autre suite à une modification continue d'un paramètre intensif externe, tel que la pression ou la température. Les transitions de premier ordre s'accompagnent d'un échange de chaleur (absorption ou dégagement) et permettent aux phases de coexister dans des proportions variables. Les transitions de second ordre, en revanche, ne génèrent pas de dégagement de chaleur et n'autorisent pas la coexistence des phases.
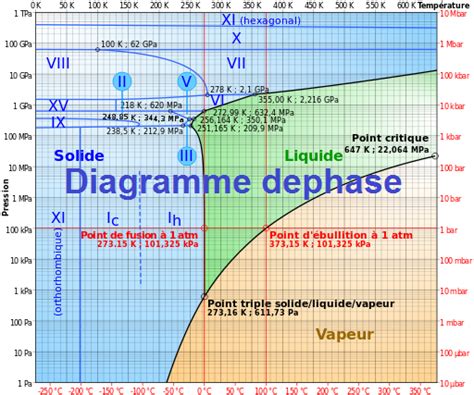
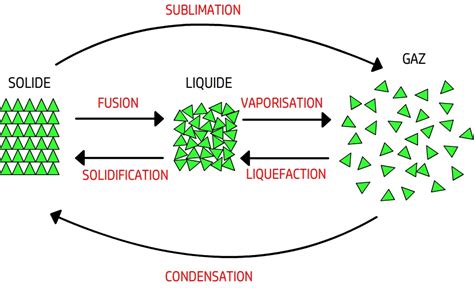
Les changements d'état classiques des corps purs (fusion, vaporisation, sublimation, solidification, liquéfaction, condensation) sont des transitions de phase du premier ordre. Ces transformations sont associées à des variations d'enthalpie et d'entropie. Par exemple, le diagramme de phases du soufre, représenté en coordonnées pression-température ((p-T)), illustre ces différentes transitions et les domaines de stabilité de chaque phase.
Considérons un gaz enfermé dans une ampoule et maintenu à une température constante (T). En faisant varier le volume du gaz à l'aide d'un piston et en mesurant la pression (p), on peut tracer l'évolution de la pression en fonction du volume. Si la température (T) est inférieure à la température critique (T_c), la pression augmente jusqu'à atteindre un plateau. Durant ce plateau, deux phases coexistent : la vapeur et le liquide. La compression entraîne un enrichissement progressif de la phase liquide.
Au début de la compression, le fluide est en phase gazeuse, qualifiée de "vapeur sèche". Dans ce cas, la variance (\mathcal{V}) (nombre de variables intensives indépendantes) est de (c+2-\varphi), où (c) est le nombre de composants et (\varphi) le nombre de phases. Pour un corps pur ((c=1)) en phase gazeuse ((\varphi=1)), (\mathcal{V}=1+2-1=2). On peut donc choisir deux variables intensives indépendantes, par exemple la température (T) et le volume massique (v). La pression (p) dépend alors de ces deux variables.
À partir d'un certain volume massique, une première goutte de liquide apparaît. La compression subséquente entraîne une diminution du volume global car le gaz se condense en liquide, qui occupe moins d'espace. Ce système biphasé (liquide-vapeur) est dit "vapeur saturante". Selon la règle de Gibbs ((\mathcal{V}=c+2-\varphi)), avec (c=1) et (\varphi=2), la variance devient (\mathcal{V}=1+2-2=1). Cela signifie que la pression (p) ne dépend plus que de la température (T), d'où l'isotherme représentée par un plateau : (p=p(T)).
La courbe marquant l'apparition de la première gouttelette de liquide est appelée courbe de rosée. La courbe où la dernière bulle de vapeur disparaît est appelée courbe d'ébullition. Ces deux courbes se rejoignent en un point singulier : le point critique, caractérisé par les coordonnées ((Tc, pc, vc)). Au-delà de la température critique ((T > Tc)), il n'y a plus de transition de phase distincte entre liquide et gaz ; il est possible de passer continûment de l'état gazeux à l'état liquide en franchissant le point critique. La pression de vapeur saturante augmente avec la température.
Les diagrammes d'état, tels que les diagrammes (p-T), (p-V), ou (T-v), sont des représentations graphiques précieuses pour visualiser les phases et les transitions d'un corps pur.
Si l'on refroidit de manière isobare un liquide, on observe l'apparition d'un germe solide à une certaine température, marquant le début de la solidification. Cette température, appelée température de solidification, ne dépend que de la pression (variance (\mathcal{V}=1)). En répétant cette mesure pour différentes pressions, on peut tracer la courbe d'équilibre liquide-solide ((p_{(\text{s})} \rightleftharpoons (\ell)} = g(T))). Cette courbe est généralement quasi verticale avec une pente positive, signifiant qu'une augmentation de pression stabilise la phase solide.
La courbe de fusion coupe la courbe de vaporisation au point triple, un point unique où les trois phases (solide, liquide, gaz) coexistent en équilibre thermodynamique. Les diagrammes (p-T) et (p-V) sont des projections d'une surface d'état tridimensionnelle.
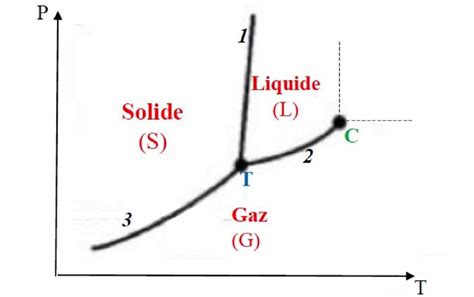
L'étude de l'équilibre liquide-vapeur devient plus complexe lorsqu'il s'agit de mélanges. Pour un système binaire, cet équilibre peut être représenté par des "lentilles d'équilibre" :
L'égalité des fugacités de chaque constituant entre les phases liquide et vapeur est la condition fondamentale de l'équilibre :[fi^{(L)}(T,P,\mathbf{x}) = fi^{(V)}(T,P,\mathbf{y}) \qquad \forall i=1, \ldots, c]où (fi^{(L)}) et (fi^{(V)}) sont les fugacités du constituant (i) dans la phase liquide et vapeur, respectivement, (T) est la température, (P) la pression, (\mathbf{x}) le vecteur des fractions molaires dans le liquide, et (\mathbf{y}) le vecteur des fractions molaires dans la vapeur.
Dans la phase liquide, la fugacité du constituant (i) peut être exprimée comme :[fi^{(L)} = \gammai xi fi^{(L,pur)} \approx \gammai xi Pi^{(s)}]où (\gammai) est le coefficient d'activité, reflétant les interactions moléculaires spécifiques dans le mélange, et (P_i^{(s)}) est la pression de vapeur saturante du corps pur (i).
Dans la phase vapeur, en négligeant les interactions intermoléculaires (hypothèse du gaz parfait), la fugacité est égale à la pression partielle : (fi^{(V)} = P yi).
L'enthalpie libre d'excès, (g^E (T,P,\mathbf{x})), est une fonction clé pour décrire les déviations par rapport au comportement idéal des mélanges :[g^E = RT \sum{i=1}^c xi \ln\gammai]Les coefficients d'activité sont dérivés de cette fonction :[RT \ln \gammai = \left( \frac{\partial Ng^E}{\partial Ni}\right){T,P,N_{j \neq i}}]
Plusieurs modèles sont utilisés pour représenter analytiquement (g^E) et prédire les diagrammes d'équilibre :
Une approche alternative consiste à utiliser une équation d'état unique valide pour les deux phases (liquide et vapeur), de la forme (P=P(T,V,\mathbf{N})). La fugacité du constituant (i) dans la phase (\phi) est alors exprimée comme :[fi^{(\phi)} = \varphii^{(\phi)} P xi^{(\phi)}]où (\varphii^{(\phi)}) est le coefficient de fugacité, calculable à partir de l'équation d'état. L'équation de Redlich-Kwong-Soave (RKS) est un exemple d'équation d'état souvent employée dans ce contexte.
Les changements de phase s'accompagnent de transferts thermiques, appelés chaleurs latentes. La chaleur latente de changement d'état (L_{1\to 2}) est la quantité de chaleur à fournir (ou à retirer) pour transformer une unité de substance de la phase 1 à la phase 2 à température et pression constantes.
Les transformations inverses (solidification, liquéfaction, condensation) s'accompagnent de dégagements de chaleur d'égale magnitude mais de signe opposé. Ces transferts thermiques peuvent être mesurés par calorimétrie. Par exemple, pour déterminer la chaleur latente de fusion de l'eau, on mélange une masse de liquide à une masse de glace dans un calorimètre et on mesure la température finale d'équilibre après fusion complète.
La relation entre la chaleur latente et le changement d'entropie lors d'une transition de phase réversible à pression constante et température (T) est donnée par :[\Delta S = \frac{L}{T}]Pour l'eau à pression atmosphérique, la chaleur latente de fusion est d'environ 334 kJ/kg, et la chaleur latente de vaporisation est d'environ 2260 kJ/kg. Ces valeurs élevées expliquent pourquoi les changements d'état ont un rôle majeur dans les transferts de chaleur naturels et artificiels.
Le dibrome ((\mathrm{Br_2})) est une substance qui, à température ambiante (25°C) et pression atmosphérique, existe principalement sous forme liquide, mais avec une pression de vapeur non négligeable. Son point d'ébullition à pression atmosphérique est d'environ 59°C. À 25°C, il est donc dans un état où l'équilibre liquide-vapeur est significatif.
La pression de vapeur saturante du dibrome à 25°C est une donnée expérimentale cruciale pour caractériser cet équilibre. Bien que les données précises ne soient pas fournies dans l'extrait, on peut supposer qu'elle est de l'ordre de quelques centaines de millibars. La compréhension de cette pression de vapeur est essentielle pour des applications telles que le stockage sécurisé du dibrome ou sa manipulation dans des réacteurs chimiques.
Les méthodes de calcul basées sur la thermodynamique, comme celles développées dans le mémoire mentionné, permettent de prédire l'énergie libre de Gibbs d'un système binaire ou ternaire, même à température et pression variables. Ces méthodes sont particulièrement utiles pour obtenir des données d'équilibre liquide-vapeur lorsque les mesures expérimentales sont difficiles ou coûteuses.
Les recherches actuelles visent à améliorer la précision et la portée des méthodes existantes. Le développement d'une méthode numérique pour calculer l'énergie libre de Gibbs de systèmes binaires et ternaires, applicable à température et pression variables, représente une avancée significative. Cette méthode permet de traiter des cas particuliers où la température ou la pression est constante.
Pour les systèmes ternaires, où la différence entre les points d'ébullition des composants peut être importante, de nouvelles approches de calcul sont proposées. Ces méthodes visent à surmonter les difficultés rencontrées par les approches classiques. De plus, de nouveaux tests de consistance pour les systèmes ternaires ont été développés, démontrant un avantage certain par rapport aux méthodes antérieures.
Un autre domaine de développement concerne les ébulliomètres. Un nouveau modèle a été mis au point pour mesurer la température d'ébullition en fonction de la pression et de la concentration de la phase liquide. Ce dispositif innovant permet de minimiser les erreurs introduites par les anciens ébulliomètres, notamment lorsque les différences de température d'ébullition entre les composants sont importantes, car il tient compte des variations de concentration de la phase liquide au cours de l'expérimentation. La précision de ce nouveau modèle a été validée par comparaison avec des données de la littérature.
La maîtrise de l'équilibre liquide-vapeur est indispensable dans de nombreux procédés industriels :
L'étude approfondie de systèmes tels que le dibrome, ou des mélanges ternaires complexes comme ceux listés dans l'abstract (par exemple, Méthyl Éthyl Cétone - Isopropanol - N-Pentyl Alcool), contribue à élargir notre connaissance des comportements thermodynamiques et à développer des modèles plus précis, essentiels pour l'ingénierie des procédés.
La compréhension des changements de phase et des propriétés thermodynamiques associées est la pierre angulaire de nombreuses applications technologiques, notamment dans le domaine des machines thermiques. Ces principes fondamentaux, appliqués à des substances spécifiques comme le dibrome, permettent d'optimiser les performances et la sécurité des installations industrielles.
tags: #equilibre #liquide #vapeur #dibrome #25c #identite