La préparation d'une boisson à partir d'un sirop concentré, comme le sirop de grenadine, est un processus familier. Cependant, derrière cette apparente simplicité se cachent des principes thermodynamiques fondamentaux qui régissent le comportement des solutions diluées. Comprendre ces principes est essentiel pour maîtriser la qualité et la consistance du produit final, qu'il s'agisse d'un sirop d'érable artisanal ou d'une boisson sucrée maison. Cet article explore les concepts clés de la thermodynamique des solutions, en se concentrant sur la manière dont la température, la concentration et les propriétés intrinsèques des composants influencent le processus de dilution et de finition du sirop.

Avant de plonger dans les spécificités de la dilution des sirops, il est crucial de comprendre les notions de capacités calorifiques. La thermodynamique définit les capacités calorifiques comme les dérivées partielles des grandeurs d'état (U) (énergie interne) et (H) (enthalpie) par rapport à la température. Plus précisément, la capacité calorifique à volume constant est exprimée par (\mathbf{\Big(\frac{\partial U}{\partial T}\Big)V=CV}), tandis que la capacité calorifique à pression constante est donnée par (\mathbf{\Big(\frac{\partial H}{\partial T}\Big)p=Cp}). Ces définitions visent à clarifier le vocabulaire et à dissiper les confusions potentielles, car le même symbole ((Cp) ou (CV)) est utilisé indépendamment du type de capacité calorifique.
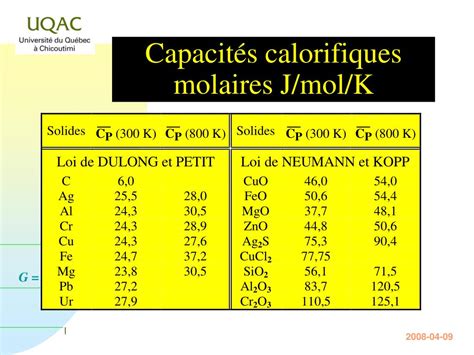
La capacité calorifique d'un système est définie comme la quantité de chaleur nécessaire pour élever sa température de 1°C. Elle s'exprime en unités d'énergie par degré, soit en Joules par Kelvin (J.K⁻¹) dans le Système International. Par exemple, un système de 200 g d'eau liquide à 25°C possède une capacité calorifique de 836 J.K⁻¹. Cette capacité calorifique est une propriété extensive, c'est-à-dire qu'elle dépend de la taille du système et est additive. Si un système est composé de plusieurs constituants, sa capacité calorifique totale est la somme des capacités calorifiques de chaque partie. Par exemple, si le système inclut 400 g d'eau liquide à 25°C dans un récipient en verre, sa capacité calorifique sera la somme de celle de l'eau et de celle du verre.
Il est important de distinguer la capacité calorifique d'un système de la capacité calorifique molaire et de la capacité calorifique massique. La capacité calorifique molaire, exprimée en J.mol⁻¹.K⁻¹, concerne une mole d'un composé. Parfois appelée "chaleur spécifique molaire", elle est, pour l'eau liquide à 25°C, de 75,2 J.mol⁻¹.K⁻¹. Cette valeur est compatible avec la capacité calorifique d'une masse donnée d'eau : pour 200 g d'eau (environ 200/18 moles), la capacité calorifique (C_p) est de 836 J.K⁻¹, ce qui se retrouve par le calcul (75,2 \times \frac{200}{18}).
La capacité calorifique massique, quant à elle, est définie par unité de masse, s'exprimant en J.kg⁻¹.K⁻¹ ou J.g⁻¹.K⁻¹. Pour l'eau liquide à 25°C, elle vaut 4180 J.kg⁻¹.K⁻¹ ou 4,18 J.g⁻¹.K⁻¹. Historiquement, l'ancienne unité d'énergie, la calorie, était définie à partir de la capacité calorifique massique d'un gramme d'eau.
La capacité calorifique d'un instrument comme un calorimètre est généralement faible, de l'ordre de quelques dizaines de Joules. Sa détermination relève de mesures expérimentales et de calculs spécifiques. La "valeur en eau" d'un calorimètre représente la masse d'eau qui aurait la même capacité calorifique que le calorimètre vide.
La préparation d'une boisson S à partir d'un sirop concentré So implique une dilution. Le facteur de dilution (F) est une mesure de la concentration du soluté dans la solution finale par rapport à la solution initiale. Il peut être exprimé en fonction du volume final de la boisson (V) et du volume initial de sirop. Si (Vs) est le volume de sirop pur et (Vw) le volume d'eau ajouté, alors le volume total de la boisson (V = Vs + Vw). Le facteur de dilution, dans ce contexte, peut être défini comme le rapport entre le volume final et le volume initial de sirop, soit (F = \frac{V}{Vs}). Alternativement, si l'on considère la concentration massique ou molaire, le facteur de dilution peut être défini comme le rapport entre la concentration initiale et la concentration finale. Par exemple, si (Ci) est la concentration initiale du sirop et (Cf) la concentration finale après dilution, alors (F = \frac{Ci}{C_f}).
L'objectif est d'atteindre une concentration désirée pour la boisson finale. Dans le cas de la préparation d'une boisson à partir d'un sirop de grenadine, on souhaite obtenir un équilibre gustatif agréable, où le goût de la grenadine est présent mais non écrasant. Le facteur de dilution permet de quantifier précisément la quantité de liquide (généralement de l'eau) à ajouter pour atteindre ce résultat.
La finition d'un sirop, particulièrement dans le contexte de la production de sirop d'érable, présente des défis techniques liés à la mesure précise de la densité et de la température. L'expérience rapportée par les producteurs met en lumière ces difficultés. Atteindre une température spécifique, par exemple 7 degrés F au-dessus du point d'ébullition, peut être délicat. L'utilisation d'un hydrotherme (un type de densimètre) pour mesurer la densité (exprimée en degrés Brix) peut devenir problématique si l'instrument coule au fond du récipient.
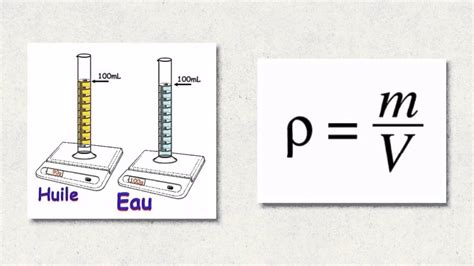
Plusieurs raisons peuvent expliquer ce phénomène. Premièrement, si le sirop est trop clair ou pas assez épais, l'hydrotherme, conçu pour flotter dans une solution d'une certaine densité, peut couler. La densité du sirop est directement liée à sa concentration en sucres. Un sirop "trop clair" signifie une concentration en sucres insuffisante par rapport à l'eau contenue. Les spécifications d'un hydrotherme indiquent souvent des plages de température pour les mesures : par exemple, 59 Brix à l'ébullition et 66 Brix à froid. Ignorer ces indications peut mener à des mesures erronées.
La température de mesure est critique. Un thermomètre de cuisson peut fournir une indication de la température, mais la mesure de densité avec un hydrotherme doit être adaptée à cette température. Il est souvent nécessaire d'attendre que la température du sirop descende pour que l'hydrotherme flotte correctement. Le débat porte sur la méthode : bouillir par petites tranches, arrêter le brûleur pour mesurer, puis recommencer ? Ou une autre approche ?
Les producteurs expérimentés recommandent plusieurs pratiques. Yves, avec ses 12 ans d'expérience, souligne que si l'hydrotherme coule au fond, même dans un sirop chaud, c'est un signe que le sirop est trop clair. Il suggère de tester l'hydrotherme à des points Brix spécifiques (59 à l'ébullition, 66 à froid). Il mentionne aussi que si le sirop est trop clair (par exemple, 60 Brix à froid), il ne remontera jamais, ou alors il est "cassé", ce qui peut impliquer une dégradation des sucres. Une astuce pour vérifier l'épaisseur est de placer le sirop au congélateur : s'il gèle, c'est qu'il n'est pas assez épais.
Andres2 partage une méthode où la vérification se fait à la sortie de l'évaporateur avec un densimètre, puis avec l'hydrotherme. Il mentionne avoir coulé son sirop à 223.4°F pour obtenir le bon degré Brix, indiquant que la température de cuisson peut varier.
Gisse, utilisant un hydrotherme depuis plus de 15 ans, recommande de couler le sirop directement dans le "sirotier" (un récipient isolant) lorsque le mercure atteint la surface. Pour accélérer la lecture, il garde du sirop chaud dans le récipient de mesure avec l'hydrotherme, afin d'éviter son refroidissement. Une mesure finale est prise après le transfert en bidons pour s'assurer de la densité.
La question de mélanger des sirops de densités différentes est également soulevée. Mélanger un sirop trop concentré (72 Brix) avec une nouvelle production est une option, mais la dilution avec de l'eau distillée est aussi envisagée. Cependant, la dilution avec de l'eau pose des problèmes d'uniformité et de conservation, nécessitant souvent une nouvelle étape de chauffage pour la mise en conserve. La solution la plus simple serait de réintroduire le sirop trop concentré dans l'évaporateur pour le diluer avec du produit moins cuit et le ramener au bon Brix.
Le comportement des solutions de sucres, particulièrement lors des variations de température, est influencé par la formation de liaisons hydrogène. L'eau pure présente une anomalie de densité : elle se contracte entre 0°C et +4°C avant de se dilater normalement au-delà. Cette contraction est due à la structure cristalline de la glace, qui maintient les molécules d'eau dans une configuration moins dense. Entre 0°C et +4°C, cette structure persiste partiellement dans l'eau liquide.
Dans les solutions de sucres, les molécules de sucre, riches en groupements -OH, sont susceptibles de former des liaisons hydrogène avec les molécules d'eau. Ces liaisons entrent en compétition avec celles que les molécules d'eau forment entre elles. Par conséquent, l'effet de contraction anomal entre 0°C et +4°C disparaît dans les solutions de sucres.
La fabrication d'un sirop chaud implique plusieurs étapes cruciales. Le processus débute par la dissolution du sucre dans l'eau, souvent dans un ratio de 2:1 pour obtenir une solution saturée. Le chauffage à 110-115°C est nécessaire, avec un remuage constant pour assurer une dissolution homogène et prévenir l'adhérence au fond du récipient. Des additifs peuvent être ajoutés pour ajuster la saveur ou améliorer la conservation.
Il est important de noter la teneur calorique des sirops. Un verre de 220 ml d'eau aromatisée avec un sirop classique peut contenir 40 à 50 calories. Une consommation accrue peut rapidement augmenter l'apport calorique journalier, équivalant à des repas plus consistants. Des alternatives, comme les concentrés à base de racine de réglisse, offrent des boissons savoureuses sans calories ni sucre. D'autres concentrés, à base de sucres naturellement présents dans les plantes, apportent une saveur fruitée avec très peu de calories et de sucre, contrastant fortement avec les sodas conventionnels.
La compréhension de ces principes thermodynamiques et des pratiques de production est essentielle pour quiconque souhaite maîtriser l'art de la préparation des sirops, garantissant ainsi un produit de qualité constante et répondant aux attentes des consommateurs.
tags: #debit #du #sirop #dilue #thermodynamique