La physique de la thermodynamique, bien qu'abstraite, est au cœur de notre perception quotidienne du chaud et du froid. Cette science, qui étudie les transformations impliquant des échanges d'énergie sous forme de chaleur, a connu un essor considérable, notamment lors de la révolution industrielle, donnant naissance à des innovations telles que le moteur thermique et le réfrigérateur. Pourtant, la nature physique de la température est restée longtemps mystérieuse, alors qu'elle était déjà maîtrisée par la technique, la médecine et la vie courante.
Historiquement, la chaleur a mis des siècles, voire des millénaires, à dévoiler sa véritable nature. Au cours de la seconde moitié du XVIIIe siècle, le chimiste écossais Joseph Black développa la théorie du « calorique », décrivant la chaleur comme un fluide sans masse, comparable à la lumière, capable de s'écouler des corps chauds vers les corps froids. Cependant, en 1798, le physicien Benjamin Thompson, comte Rumford, porta un coup fatal à cette théorie en mesurant la chaleur produite lors du forage de canons. Il démontra que cette chaleur était proportionnelle au travail fourni, suggérant une relation entre chaleur et travail mécanique. Parallèlement, divers inventeurs parvenaient empiriquement à extraire une « force motrice » à partir de la chaleur, comme en témoignent la marmite de Denis Papin en 1679 et la machine à vapeur de James Watt en 1769. Au XIXe siècle, le concept d'énergie, plus général que l'énergie mécanique définie au XVIIIe siècle, émergea, le terme « energy » ayant été introduit en 1802 par le physicien Thomas Young.
La température, souvent confondue avec la chaleur, est une propriété qui permet de quantifier l'agitation des particules d'une substance. Elle est mesurée par des thermomètres, dont de nombreux modèles ont été proposés au fil des générations, exploitant le phénomène de dilatation. Le thermomètre à mercure, inventé en 1742 par le Suédois Anders Celsius, fut pendant plusieurs décennies l'instrument de référence, basé sur l'échelle centigrade où le zéro correspond au point de congélation de l'eau et 100°C à son point d'ébullition sous une pression standard de 1013 hPa.
Il est crucial de distinguer la température de la sensation de chaud ou de froid. Deux corps amenés au « contact thermique », où ils peuvent échanger librement de la chaleur, évoluent spontanément jusqu'à égaliser leurs températures. Le corps le plus froid reçoit de la chaleur, tandis que le corps le plus chaud en perd. La différence de température dicte le sens de ce transfert. Cependant, la sensation que nous éprouvons n'est pas directement liée à cette différence de température.
Une expérience simple illustre ce point : placer un glaçon sur une plaque de bois et sur une plaque de fer. Bien que le bois et le métal soient à la même température ambiante, le glaçon sur le fer fondra plus rapidement. Le fer, bon conducteur thermique, absorbe la chaleur de la main et du glaçon plus efficacement que le bois, un isolant thermique. Ainsi, la sensation de froid ressentie en touchant le fer est plus intense car notre main transfère plus rapidement sa chaleur au métal. La sensation de chaud ou de froid au toucher d'un objet dépend donc de la « quantité de chaleur transférée », une notion quantifiée par la conductivité thermique.
La conductivité thermique, notée et exprimée en W/(m.°C), mesure l'aptitude d'un matériau à conduire la chaleur. Plus cette conductivité est grande, meilleur est le conducteur thermique. Inversement, un matériau à faible conductivité est un bon isolant. C'est pourquoi, lorsqu'on touche une table dont la surface est en bois et les pieds en métal, le bois semble plus chaud que le métal, même s'ils sont à la même température. Le bois, isolant, limite le transfert de chaleur de notre main, donnant une impression de chaleur. Le métal, conducteur, absorbe rapidement la chaleur de notre main, procurant une sensation de froid.
La chaleur, contrairement à la température, est un transfert d'énergie thermique entre deux systèmes de températures différentes. Elle est mesurée en joules (J). Le Joule est l'unité de travail et d'énergie dans le Système International. Il correspond au travail produit par une force de 1 Newton dont le point d'application se déplace de 1 mètre dans la direction de la force, ou plus simplement, au travail nécessaire pour soulever une masse de 100 g d'un mètre.
Lorsque deux objets de températures différentes sont mis en contact, un transfert de chaleur s'opère. L'objet chaud se refroidit, et l'objet froid se réchauffe, jusqu'à atteindre un équilibre thermique. Ce transfert d'énergie thermique se mesure par la quantité de chaleur, notée Q.
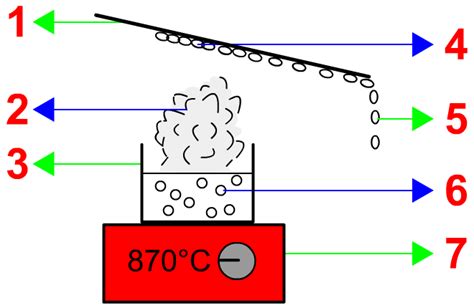
L'observation de l'eau chauffée sur une plaque de cuisson électrique ou une cuisinière à gaz offre une illustration concrète de ces principes. Initialement, l'apport de chaleur fait augmenter la température de l'eau. Cependant, aux alentours de 100°C (à pression atmosphérique normale), le point d'ébullition est atteint. À ce stade, des bulles de vapeur apparaissent, et malgré un chauffage continu, la température stagne à 100°C. Ce phénomène s'explique par le changement d'état de l'eau liquide en vapeur. La conversion d'une masse de liquide en la même masse de vapeur exige une quantité importante de chaleur, appelée chaleur latente de vaporisation, et s'effectue à température constante.
L'étude de la thermodynamique s'étend également aux systèmes ouverts, où des fluides s'écoulent à débit constant, comme dans les machines industrielles. La réécriture du premier principe de la thermodynamique permet d'établir des lois valables dans ces conditions. De plus, le second principe de la thermodynamique impose un sens aux transformations, expliquant pourquoi la chaleur se transfère spontanément du corps chaud vers le corps froid.
Le développement de la thermodynamique a permis de définir une « température absolue » T, mesurée en Kelvin (K), du nom du physicien britannique William Thomson, lord Kelvin. Contrairement à la température t en degrés Celsius, la température absolue est une mesure directe de l'état d'agitation des particules constituant la matière. Plus l'agitation est grande, plus la température est élevée. La température de 0 Kelvin, ou zéro absolu, correspondrait à l'absence totale de mouvement des particules.
Les échanges thermiques s'effectuent selon trois modes principaux :
Il est essentiel de comprendre que nous ne ressentons pas directement le froid ou le chaud, mais plutôt les échanges thermiques. Quand notre corps évacue de l'énergie thermique, nous avons froid ; quand il en reçoit, nous avons chaud. Plus le flux thermique (la quantité d'énergie échangée par unité de temps) est important, plus la sensation de chaud ou de froid est intense.
Par exemple, à température égale, on ressent plus froid dans l'eau que dans l'air. Cela s'explique par le coefficient d'échange thermique. Le coefficient d'échange avec l'eau est beaucoup plus élevé qu'avec l'air. Ainsi, les échanges d'énergie entre notre corps et l'eau se font beaucoup plus rapidement, d'où une sensation de froid plus prononcée, même si la température de l'eau et de l'air est identique.
L'évaporation joue également un rôle crucial dans la sensation de refroidissement. Lorsque l'eau s'évapore de la peau (après une douche, par exemple), elle puise la chaleur de notre corps, provoquant une sensation de fraîcheur. C'est pourquoi s'asperger d'eau est efficace pour se rafraîchir par temps chaud.
Notre corps est capable de produire de la chaleur, un processus appelé thermogenèse. Les muscles, par exemple, libèrent environ les deux tiers de leur énergie sous forme de chaleur. C'est pourquoi les femmes, ayant généralement moins de masse musculaire que les hommes, peuvent ressentir le froid plus rapidement. L'organisme cherche à maintenir une température interne stable, notamment celle des organes vitaux. En cas de froid, il peut réduire l'apport sanguin aux extrémités pour préserver la chaleur au centre du corps.
L'alimentation peut également influencer notre température interne. Certaines épices comme la cannelle, le clou de girofle, le gingembre ou le piment peuvent stimuler la production de chaleur par le corps (thermogenèse postprandiale) en agissant sur la circulation sanguine et en activant certaines hormones.
Le secteur textile joue un rôle important dans notre confort thermique, proposant des fibres de plus en plus performantes. Des matériaux comme la polaire, l'alpaga, la soie ou la laine offrent d'excellentes propriétés isolantes et régulatrices. L'alpaga, par exemple, est cinq fois plus chaud que la laine classique tout en étant plus léger et doux, grâce à de minuscules poches d'air dans ses fibres. La soie est particulièrement régulatrice pour les personnes qui transpirent beaucoup.
L'environnement de vie a également un impact sur notre ressenti thermique. Il est recommandé de maintenir des températures adaptées à chaque pièce de la maison pour optimiser le confort et réduire la consommation d'énergie. Par exemple, une température de 15 à 18°C est idéale pour les chambres à coucher, favorisant un bon sommeil et la combustion des graisses. La salle de bain peut être plus chaude (environ 24°C) pour éviter les frissons après la douche.
La thermodynamique est également au cœur des débats actuels sur le changement climatique. L'utilisation d'énergies renouvelables est une piste pour limiter le réchauffement, mais les opinions divergent quant à l'influence humaine sur ce phénomène. La science continue d'explorer ces questions complexes, tandis que la poésie rappelle l'importance de la chaleur humaine.
Il est intéressant de noter que les couleurs peuvent également influencer notre perception de la chaleur. Le rouge est associé à la chaleur, tandis que le bleu est perçu comme une couleur froide. Ces associations psychologiques peuvent affecter notre humeur et notre sensibilité aux variations de température.
La compréhension de la thermodynamique, de la différence entre chaleur et température, et des mécanismes des transferts thermiques nous permet d'expliquer de nombreux phénomènes de notre quotidien, depuis la sensation de froid au toucher d'un objet jusqu'aux phénomènes d'ébullition. Cette science fondamentale continue d'évoluer, nous offrant des clés pour mieux appréhender notre environnement et relever les défis énergétiques de demain.
tags: #correction #physique #thermodynamique #sensation #de #chaud