L'effet thermodynamique, au cœur de la physique et de l'ingénierie thermique, est une notion fondamentale qui régit les transformations et les échanges d'énergie au sein des systèmes. Comprendre ses principes est essentiel pour analyser les processus thermiques, concevoir des machines performantes et optimiser les rendements énergétiques dans une multitude d'applications industrielles et technologiques. Cet article explore en profondeur la définition de l'effet thermodynamique, ses lois fondamentales, les cycles qui le décrivent, et ses manifestations concrètes à travers divers exemples.
L'effet thermodynamique se définit comme l'ensemble des changements énergétiques, impliquant principalement la chaleur et le travail, qui surviennent lors des transformations subies par un système. L'étude de ces échanges est cruciale pour l'analyse des processus thermiques et la conception des machines thermiques, qu'il s'agisse de moteurs, de réfrigérateurs ou de centrales électriques.
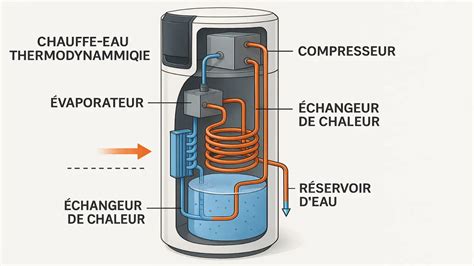
La thermodynamique, cette branche de la physique qui étudie les échanges d'énergie, notamment sous forme de chaleur, et les transformations de cette énergie dans les systèmes, repose sur des principes fondamentaux. Ces principes, tels que la conservation de l'énergie et l'irréversibilité des processus, permettent d'expliquer le comportement des systèmes à l'échelle macroscopique.
L'énergie, notion familière, se manifeste sous des formes variées : énergie thermique (chaleur), énergie cinétique (liée au mouvement), énergie rayonnante (lumière), énergie chimique (contenue dans les carburants ou les aliments), énergie potentielle (comme celle d'une masse d'eau derrière un barrage), énergie électrique, et bien d'autres. La thermodynamique s'intéresse à la manière dont ces formes d'énergie sont échangées et converties.
Historiquement, l'énergie utilisée par l'homme était principalement celle issue de son travail physique, puis celle du feu, du vent et de l'eau. La fin du XVIIIe siècle a marqué un tournant avec l'avènement de la machine à vapeur, alimentée par le charbon, révolutionnant l'industrie. Plus tard, la fin du XIXe siècle a vu l'essor de l'électricité, permettant une distribution d'énergie sans précédent. Ces découvertes ont initié des révolutions industrielles et sociales majeures, transformant notre rapport à l'énergie.
Il est possible de transformer une forme d'énergie en une autre. Par exemple, l'énergie chimique de l'essence est convertie en énergie mécanique dans un moteur de voiture. L'énergie rayonnante du soleil est transformée en chaleur. La chaleur d'une chaudière peut devenir de l'énergie mécanique grâce à une machine à vapeur. Toutes les formes d'énergie peuvent, en principe, être converties en électricité.
Cependant, ces transformations ne sont pas arbitraires et sont régies par des lois fondamentales.
Les concepts de base en thermodynamique relatifs à l'effet incluent plusieurs lois et principes qui guident les analyses énergétiques et les transformations physiques.
La Première Loi de la Thermodynamique : Le Principe de Conservation de l'Énergie
Également connue sous le nom de principe de conservation de l'énergie, cette loi stipule que l'énergie totale d'un système isolé reste constante. L'énergie ne peut être ni créée ni détruite, mais seulement transformée ou transférée d'un système à un autre. Elle peut être exprimée par l'équation fondamentale :[ \Delta U = Q - W ]où ( \Delta U ) représente la variation de l'énergie interne du système, ( Q ) est la chaleur ajoutée au système, et ( W ) est le travail effectué par le système. Cette loi est universellement applicable, qu'il s'agisse de réactions chimiques, de processus physiques ou de fonctionnement de machines.

La Deuxième Loi de la Thermodynamique : L'Entropie et l'Irréversibilité
La deuxième loi de la thermodynamique introduit le concept d'entropie, une mesure du désordre ou du chaos d'un système au niveau microscopique. Elle suggère que l'énergie totale dissipée sous forme de chaleur ne peut pas être complètement convertie en travail utile. Cette loi est souvent exprimée par l'augmentation de l'entropie totale lors d'un processus spontané. Mathématiquement, pour un processus réversible, elle peut être formulée comme ( \Delta S = \frac{Q{rev}}{T} ), où ( \Delta S ) est la variation d'entropie, ( Q{rev} ) la chaleur échangée de manière réversible, et ( T ) la température absolue.
L'entropie (( S )) est un indicateur de désordre. Un système isolé évolue spontanément vers un état de désordre croissant, c'est-à-dire une augmentation de son entropie. Cette loi a des implications profondes, notamment en expliquant pourquoi aucune machine thermique ne peut avoir une efficacité de 100 %.
Le Troisième Principe de la Thermodynamique
Le troisième principe stipule qu'un cristal parfait à la température du zéro absolu (0 Kelvin, soit -273,15 °C) possède une entropie nulle. À cette température, tous les atomes sont parfaitement ordonnés et immobiles.
Plusieurs grandeurs sont essentielles à la compréhension des effets thermodynamiques :
Un cycle thermodynamique désigne une série de transformations successives subies par un système qui, au terme de ces transformations, revient à son état initial. Ces cycles sont au cœur du fonctionnement de nombreuses machines thermiques.
Le cycle de Carnot est un modèle théorique de cycle thermodynamique réversible, composé de quatre transformations : deux expansions et deux compressions, réalisées entre deux réservoirs thermiques à des températures distinctes.
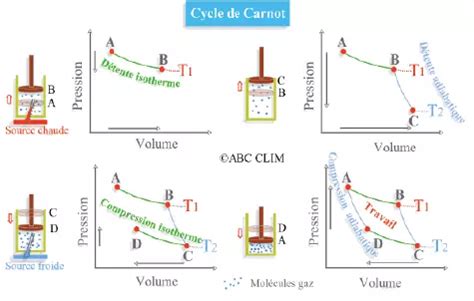
L'efficacité théorique du cycle de Carnot, qui représente le rendement maximal possible pour une machine thermique opérant entre deux températures données, est donnée par la formule :[ \eta = 1 - \frac{TC}{TH} ]où ( TC ) et ( TH ) sont les températures absolues des réservoirs froid et chaud, respectivement.
Par exemple, si une machine thermique opère entre 500 K et 300 K, son efficacité de Carnot maximale est de ( 1 - \frac{300}{500} = 0.4 ), soit 40 %. Bien que ce cycle soit idéal et irréalisable en pratique en raison des irréversibilités (frottements, transferts de chaleur non parfaits), il sert de référence fondamentale pour évaluer les performances des moteurs thermiques réels.
Le cycle de Rankine est un cycle thermodynamique couramment utilisé dans les centrales électriques à vapeur pour convertir la chaleur en travail mécanique. Il est similaire au cycle de Carnot mais inclut des processus non réversibles qui le rendent plus pratique pour les applications industrielles.
Les étapes principales du cycle de Rankine sont :
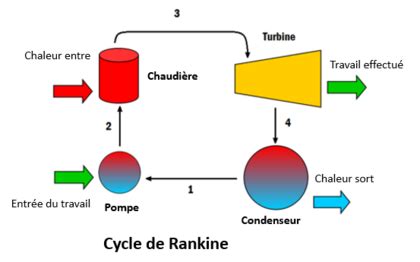
L'efficacité du cycle de Rankine dépend de la différence de température entre la source chaude (vapeur à haute température) et la source froide (eau de condensation). Bien qu'il soit moins efficace que le cycle de Carnot idéal, sa mise en œuvre est plus réaliste dans les centrales électriques.
Les cycles thermodynamiques sont également la base du fonctionnement des réfrigérateurs et des pompes à chaleur. Contrairement aux moteurs thermiques qui convertissent la chaleur en travail, ces systèmes utilisent du travail pour transférer la chaleur d'un endroit à un autre.
Dans un réfrigérateur, le cycle vise à extraire de la chaleur d'un espace froid (l'intérieur du réfrigérateur) pour la rejeter dans un environnement plus chaud (la cuisine). Dans une pompe à chaleur, le processus est inversé : elle extrait de la chaleur d'une source froide (l'air extérieur, le sol) pour chauffer un espace plus chaud (une maison).
Le Coefficient de Performance (COP) est la mesure clé de l'efficacité de ces appareils. Pour une pompe à chaleur, il est défini comme le rapport entre la chaleur utile délivrée et le travail consommé :[ COP{chauffage} = \frac{Q{chaud}}{W} ]Pour un réfrigérateur, il s'agit du rapport entre la chaleur extraite de la source froide et le travail consommé :[ COP{refroidissement} = \frac{Q{froid}}{W} ]Un COP élevé indique une meilleure efficacité. Par exemple, une pompe à chaleur avec un COP de 4 fournit 4 unités de chaleur pour chaque unité de travail consommée.
Les étapes typiques d'un cycle frigorifique comprennent la compression du fluide frigorigène (qui augmente sa température), sa condensation (libération de chaleur), sa détente (chute de température) et son évaporation (absorption de chaleur).
L'effet thermodynamique est omniprésent et trouve des applications dans presque tous les domaines de l'ingénierie et de la vie quotidienne.
En génie chimique, la compréhension de l'effet thermodynamique est cruciale pour :
Par exemple, la combustion du méthane (( \text{CH}4 + 2 \text{O}2 \rightarrow \text{CO}2 + 2 \text{H}2\text{O} )) est une réaction exothermique (( \Delta H < 0 )) qui libère une quantité significative d'énergie thermique, utilisable pour produire du travail.
Le potentiel chimique (( \mu )) est une extension de l'enthalpie et de l'entropie pour les systèmes ouverts. Il représente l'énergie ajoutée à un système par l'ajout d'une mole d'un constituant et aide à prédire les variations de composition à l'équilibre :[ \mu = \left( \frac{\partial G}{\partial n} \right)_{T,P} ]
Dans le génie mécanique, l'effet thermodynamique est fondamental pour :
La chaleur latente de vaporisation joue un rôle clé dans les machines frigorifiques et les centrales électriques. Par exemple, l'énergie nécessaire pour vaporiser de l'eau est donnée par ( Q = m \times L ), où ( L ) est la chaleur latente de vaporisation.
Même en génie civil, la thermodynamique intervient, notamment dans la conception de bâtiments économes en énergie. L'isolation thermique des murs, des fenêtres et des toitures vise à minimiser les transferts de chaleur entre l'intérieur et l'extérieur, réduisant ainsi les besoins en chauffage et climatisation.
Pour mieux appréhender l'effet thermodynamique, la résolution d'exercices pratiques est indispensable.
Un exercice typique pourrait impliquer le calcul du travail effectué et de l'entropie générée par une chaudière opérant entre deux réservoirs de chaleur à des températures spécifiques, en utilisant les données fournies et les formules appropriées.
L'effet thermodynamique, régi par des lois fondamentales telles que la conservation de l'énergie et le principe d'augmentation de l'entropie, est un pilier de la compréhension des phénomènes physiques et de la conception de systèmes énergétiques. Des cycles idéaux comme celui de Carnot aux applications industrielles concrètes comme le cycle de Rankine, en passant par le fonctionnement des réfrigérateurs et des pompes à chaleur, les principes thermodynamiques sous-tendent une vaste gamme de technologies essentielles à notre société. Maîtriser ces concepts permet non seulement d'expliquer le monde qui nous entoure, mais aussi d'innover pour un avenir plus efficace et durable sur le plan énergétique.
tags: #comment #trouver #le #cycle #de #reaction