En physique, et plus particulièrement en thermodynamique, les coefficients calorimétriques et thermoélastiques sont des coefficients permettant d'exprimer, pour les premiers, la chaleur absorbée par un système thermodynamique et, pour les seconds, les variations de volume et de pression de ce système. Ces coefficients sont définis pour les corps purs comme pour les mélanges. Ces coefficients sont liés aux potentiels thermodynamiques, dont ils sont les dérivées secondes. Il est ainsi possible d'établir le signe des capacités thermiques et des coefficients de compressibilité, ainsi que diverses relations, notamment les relations de Clapeyron, relation de Mayer et relation de Reech. Les coefficients calorimétriques sont liés aux variations de l'entropie du système.
Le coefficient de compressibilité isentropique, noté $\chi_s$, est une grandeur intensive exprimée en Pa⁻¹. Il quantifie la variation relative de volume d'un système thermodynamique sous l'effet d'une variation de pression, lorsque le processus se déroule à entropie constante. Contrairement à la compressibilité isotherme, la compressibilité isentropique considère un système isolé de son environnement thermique, où aucune chaleur n'est échangée.
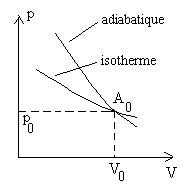
Les coefficients thermoélastiques, tels que le coefficient de compressibilité isentropique, sont issus de l'étude des relations entre la pression, le volume et la température d'un système. Ils sont intimement liés aux potentiels thermodynamiques. Pour un système dont les seules variables pertinentes sont la pression ($p$), le volume ($V$) et la température ($T$), ces coefficients peuvent être exprimés comme des dérivées partielles secondes des potentiels thermodynamiques.
Les potentiels thermodynamiques fondamentaux sont :
où $S$ représente l'entropie et $T$ la température absolue.
Les coefficients calorimétriques et thermoélastiques peuvent être exprimés comme des dérivées partielles secondes de ces potentiels par rapport à leurs variables naturelles. Par exemple, l'énergie interne ($U$) a pour variables naturelles l'entropie ($S$) et le volume ($V$). L'enthalpie ($H$) a pour variables naturelles l'entropie ($S$) et la pression ($p$). L'énergie libre de Helmholtz ($F$) a pour variables naturelles la température ($T$) et le volume ($V$). L'enthalpie libre de Gibbs ($G$) a pour variables naturelles la température ($T$) et la pression ($p$).
Dans ce contexte, le coefficient de compressibilité isentropique $\chi_s$ est défini comme :
$$ \chis = -\frac{1}{V} \left( \frac{\partial V}{\partial p} \right){S} $$
où $V$ est le volume, $p$ la pression et $S$ l'entropie. Le signe négatif est introduit pour que $\chi_s$ soit généralement positif, car une augmentation de pression ($dp > 0$) entraîne une diminution de volume ($dV < 0$) pour un corps stable.
La compressibilité isentropique est étroitement liée à la compressibilité isotherme ($\chi_T$), définie par :
$$ \chiT = -\frac{1}{V} \left( \frac{\partial V}{\partial p} \right){T} $$
La relation entre les deux est donnée par :
$$ \chis = \chiT \frac{Cp}{Cv} $$
où $Cp$ est la capacité thermique isobare et $Cv$ est la capacité thermique isochore. Cette relation met en évidence que la compressibilité isentropique est toujours supérieure ou égale à la compressibilité isotherme, car le rapport des capacités thermiques ($Cp/Cv$), souvent noté $\gamma$ (ou $\kappa$), est supérieur ou égal à 1.
Le rapport des capacités thermiques, $\gamma = Cp / Cv$, joue un rôle crucial dans la détermination de la compressibilité isentropique. Pour les gaz parfaits, ce rapport dépend de l'atomicité des molécules :
Pour les gaz parfaits, la relation entre les coefficients calorimétriques et thermoélastiques est particulièrement simple. Par exemple, la relation de Mayer relie $Cp$ et $Cv$ à la constante universelle des gaz parfaits ($R$) :
$$ Cp - Cv = R $$
En divisant par $C_v$, on obtient :
$$ \frac{Cp}{Cv} - 1 = \frac{R}{C_v} $$
Soit :
$$ \gamma - 1 = \frac{R}{C_v} $$
D'où :
$$ \gamma = 1 + \frac{R}{C_v} $$
Pour un gaz parfait, $Cv$ ne dépend que de la température. Ainsi, $\gamma$ dépend également de la température. Les capacités thermiques dépendent de la température, des différences apparaissent avec l'atomicité. Une atomicité supérieure entraîne des résultats plus complexes. Ils dépendent de la forme de la molécule et de son atomicité. Pour un gaz parfait, $Cv$ est une fonction de $T$ seule. La relation de Mayer $Cp - Cv = R$ est valable, quelque soit le gaz. La capacité thermique isochore $C_v$ est nulle pour un gaz parfait. L'énergie interne $U$ ne dépend que de la température pour un gaz parfait.
Pour un gaz parfait, le coefficient de compressibilité isentropique est directement lié au rapport des capacités thermiques :
$$ \chi_s = \frac{1}{\gamma p} $$
Dans ce cas, $\gamma$ est une fonction de la température. Si l'on considère un gaz parfait de Laplace, où $\gamma$ est constant, alors $\chi_s$ est inversement proportionnel à la pression. Les lois de Laplace décrivent les transformations adiabatiques réversibles. Dans une transformation adiabatique réversible, la relation $pV^\gamma = \text{constante}$ est vérifiée. Après intégration, on trouve que $\gamma \ln(V) + \ln(p) = \text{Cte}$. Autrement dit, la quantité $pV^\gamma$ reste constante au cours de la transformation. Par ailleurs, la quantité de matière étant fixée, le produit $pV/T$ reste également constant. On en déduit que les produits $TV^{\gamma-1}$ et $T^\gamma p^{1-\gamma}$ sont invariants pendant la transformation.
L'expérience de Clément et Desormes a permis de mesurer $\gamma$ pour l'air. Le principe consiste à faire entrer dans un ballon en verre de l'air sous pression. Après avoir attendu l'équilibre thermique, on note la surpression initiale $\delta p1$. On ouvre ensuite un robinet pour que l'air sous pression s'échappe du ballon, puis on referme le robinet. L'air qui reste a subi une détente adiabatique quasi réversible. L'air dans le ballon s'est donc refroidie. En s'équilibrant avec l'extérieur, le gaz voit sa température et donc sa pression augmenter. On note $\delta p2$ la surpression finale. À 20°C et sous 1 atm, on a mesuré que le son se propage à la vitesse $c{\text{son}} = 343,4 \, \text{m.s}^{-1}$ dans l'air. La vitesse du son dans un gaz est donnée par $c{\text{son}} = \sqrt{\gamma RT/M}$, où $R$ est la constante des gaz parfaits, $T$ la température et $M$ la masse molaire.
Pour les gaz réels, la relation est plus complexe. Le facteur de compressibilité $Z = pV/(RT)$ n'est pas égal à 1. Le coefficient de compressibilité isentropique peut être exprimé en fonction de $Z$ et de ses dérivées. Aux basses pressions et températures, le comportement se rapproche de celui des gaz parfaits. Cependant, à des pressions et températures plus élevées, les interactions moléculaires deviennent significatives, modifiant la compressibilité.
La plupart des gaz réels se refroidissent dans une détente isoénergétique (effet Joule), quelle que soit la température initiale. Pour un gaz réel, le coefficient de Joule-Thomson est généralement non nul.
Pour les phases condensées (liquides et solides), les coefficients $\alpha$ (dilatation isobare) et $\chi_T$ (compressibilité isotherme) sont généralement très faibles, indiquant que ces phases sont peu dilatable et peu compressible. Le coefficient de compressibilité isentropique est également faible.
Pour un solide, il est souvent supposé que le volume ne dépend pas de la température (solide indilatable) et que le module de compressibilité isostatique varie linéairement avec la pression.
Dans le cas des liquides, la capacité thermique est souvent anormalement élevée, comme pour l'eau. Le $c_p$ de l'eau est de $4,2 \, \text{J.K}^{-1}\text{.g}^{-1}$, ce qui correspond à une capacité thermique molaire de l'ordre de $75 \, \text{J.K}^{-1}\text{.mol}^{-1}$, soit trois fois plus que celle des solides.
La mesure directe du coefficient de compressibilité isentropique est moins courante que celle de la compressibilité isotherme. Cependant, elle peut être déduite de mesures de capacités thermiques ou de la vitesse du son.
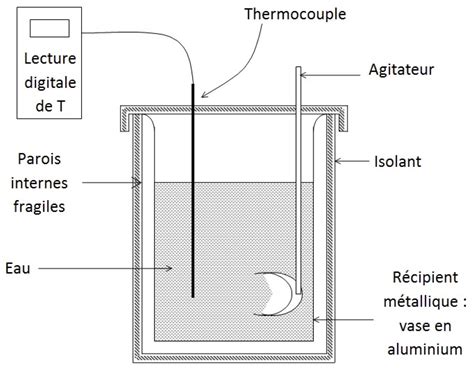
La capacité thermique isobare ($Cp$) et la capacité thermique isochore ($Cv$) peuvent être mesurées par calorimétrie. Un calorimètre est une enceinte adiabatique où les corps évoluent de façon monobare.
Pour mesurer la capacité thermique d'un solide, on peut suivre la procédure suivante : dans un vase calorimétrique de capacité $C$, on introduit une masse d'eau $me$. On attend l'équilibre thermique puis on note la température $T1$. On plonge une masse $ms$ d'un solide de capacité $cs$ inconnue, et de température $T2$. Après quelques dizaines de secondes, la température se stabilise à une température finale $Tf$.
Pour les liquides, on préfère une méthode électrique de mesure par écoulement stationnaire. Dans un tube calorifugé, on fait circuler un liquide à pression constante, en régime stationnaire de débit massique $D_m$. On plonge une résistance chauffante $R$ que l'on alimente par une source de courant d'intensité $I$. Le transfert thermique est fourni par effet Joule.
La vitesse du son dans un milieu est directement liée à sa compressibilité isentropique. La relation est la suivante :
$$ c{\text{son}} = \sqrt{\frac{1}{\rho \chis}} $$
où $\rho$ est la masse volumique du milieu et $\chis$ est le coefficient de compressibilité isentropique. En mesurant la vitesse du son et la masse volumique, on peut donc calculer $\chis$.
Le coefficient de compressibilité isentropique est un paramètre fondamental en thermodynamique, avec des applications dans divers domaines :
Bien que la thermodynamique n'interdise pas que ces coefficients soient négatifs, un corps présentant de telles propriétés serait instable considéré seul car il diminuerait l'entropie, en contradiction avec le deuxième principe de la thermodynamique. Une telle situation est donc difficilement observable. Cependant, des coefficients négatifs peuvent être observés dans un contexte impliquant des phénomènes compensant cette instabilité. La compressibilité est une propriété tensorielle, elle peut dépendre de la direction dans laquelle la force de pression est appliquée ; trois valeurs propres différentes peuvent être observées, le tenseur étant alors anisotrope. Des compressibilités négatives linéaires ou planaires sont observées sur des mousses de dicyanoaurate de zinc et des cristaux composés d'eau et de méthanol ; ce phénomène, appelé auxétisme, est expliqué par l'architecture des cristaux à l'échelle moléculaire.
Le volume d'un corps augmente généralement sous l'effet d'une augmentation de la température, aussi le coefficient de dilatation isobare est-il le plus souvent positif. Néanmoins, la relation (rs6) n'impose pas le signe de ce coefficient, qui peut donc être négatif pour un corps stable. Pour une phase idéalement indilatable ($\alpha = 0$) ou incompressible ($\chiT = 0$), la relation de Mayer conduit à la relation : $Cp - C_v = R$.
La température d'un gaz donné ne varie ni dans une détente de Joule-Gay-Lussac, ni dans une détente de Joule-Thomson. Les seules variables considérées ici sont la pression, la température et le volume, les intégrations ont été faites à quantité de matière constante. On sait néanmoins que le volume est une grandeur extensive ; par conséquent, à pression et température constantes, doubler par exemple la quantité de matière induit un doublement du volume.
Pour un solide, il est supposé que le volume ne dépend pas de la température (solide indilatable) et que le module de compressibilité isostatique varie linéairement avec la pression.
Les formules d'Ehrenfest permettent de définir l'évolution de la pression de transition de phase d'un corps pur en fonction de la température pour les transitions d'ordre 2 selon la classification d'Ehrenfest. Ces formules ne sont valables que pour une transition d'ordre 2 selon la classification d'Ehrenfest des transitions de phase, c'est-à-dire, selon la classification actuelle, pour une transition de phase n'impliquant pas une enthalpie de changement d'état.
tags: #coefficient #de #compressibilite #isentropique #thermodynamique